По данным ученых международного центра СИММИТ на пшенице встречаются 25 грибных, 3 бактериальных, 1 вирусное, 3 нематодных, 4 физиолого-генетических болезней и 8 заболеваний, обусловленных недостатком минерального питания и другими абиотическими факторами. Видовой состав возбудителей болезней озимой и яровой пшеницы особо не различается, за исключением отдельных.
Она поражается четырьмя видами головни, тремя ржавчины, мучнистой росой, септориозом и гельминтоспориозными пятнистостями, корневыми гнилями. На этой культуре встречаются: бактериальные, желтые или слизистые, базальные и вирусные болезни (Prescott et all., 1986; Койшыбаев, 2002; Dubeiller, Singh et all, 2014).
Возбудители головни и ржавчины узкоспециализированны, например, гриб Tilletia tritici паразитирует только на пшенице и не поражает другие культурные и дикорастущие злаки. В процессе длительной эволюции они приспособились к определенному растению-хозяину. В то же время возбудители бактериальных и вирусных болезней поражают большой круг культурных и дикорастущих злаков: например, вирус русской мозаики пшеницы – ячмень, рожь и просо. Широко специализированные патогены лучше выживают в природе, сохраняются на пожнивных растительных остатках и в почве, дикорастущие злаки являются часто резерваторами их инфекции.
Головневые болезни
Возбудители головни злаков относятся к семействам Tilletiacea и Ustilaginacea порядка Ustilaginales или головневых грибов. Для них характерно образование на репродуктивных или вегетативных органах растения-хозяина головневых вздутий или мешочков, состоящих из черной сажистой массы – телиоспор, которые являются покоящейся стадией гриба. У видов семейства Tilletiacea телиоспоры прорастают в одноклеточные базидии с базидиоспорами (споридии), располагающимися на их верхушке. Для представителей семейства Ustilaginacea характерно образование 4-клеточных базидий или промицелий с латеральными и верхушечным базидиоспорами [табл. 1].
Таблица 1. Видовой состав болезней пшеницы и их возбудители, поражаемые ими органы
У некоторых видов этого семейства они отсутствуют, слияние клеток противоположного пола базидий дает начало двухядерному мицелию (Шварцман,1960; Ульянищев, 1968).
На пшенице паразитируют 5 видов головневых грибов: Tilletia caries, T. levis, Ustilago tritici, Tilletia indica и Uromyces tritici, наиболее широко распространены первые два вида. Карликовая головня, несмотря на ограниченный ареал, является очень вредоносной. Инфекция головневых болезней, в основном сохраняется на поверхности или внутри семян, у некоторых видов на стерневых остатках и в почве. По характеру её передачи и особенностям заражения растений они разделяются на 3 группы.
Первая группа. Инфекция сохраняется на поверхности семян или в виде головневых примесей к ним. Телиоспоры прорастают в мицелий и проникают в колеоптиле пшеницы, далее развивается внутриклеточно, достигает конуса нарастания, превращая зачаточный колос в головневый сорус. По такому циклу развивается твердая головня пшеницы.
Вторая группа. Телиоспоры распыляются и в период цветения оседают на рыльце завязи пшеницы. При наличии капельножидкой влаги они прорастают в 4-клеточные базидии, клетки противоположного пола копулируют между собой, и образуется диплоидный мицелий, который через рыльца цветка проникает в завязь. Мицелий гриба сохраняется в зародыше зерна в покоящемся состоянии до следующего года, реже в эндосперме. Зараженные головней семена внешне не отличаются от здоровых. По такому циклу развивается возбудитель пыльной головни.
Третья группа. По циклу развития особо выделяется карликовая головня. Возбудитель сохраняется в почве, телиоспоры прорастают в мицелий и заражают всходы с момента прорастания семян до кущения. Заболевание передается также семенами, которые заспоряются при уборке, телиоспоры в почве не теряют жинеспособность до 5-7 лет.
Твердая (мокрая) головня
Возбудителями болезни твердой головни пшеницы являются грибы: Tilletia caries (DC) Tul. (син.: Tilletia foetidia Liro) и Tilletia levis (син.: Tilletia tritici Wint).
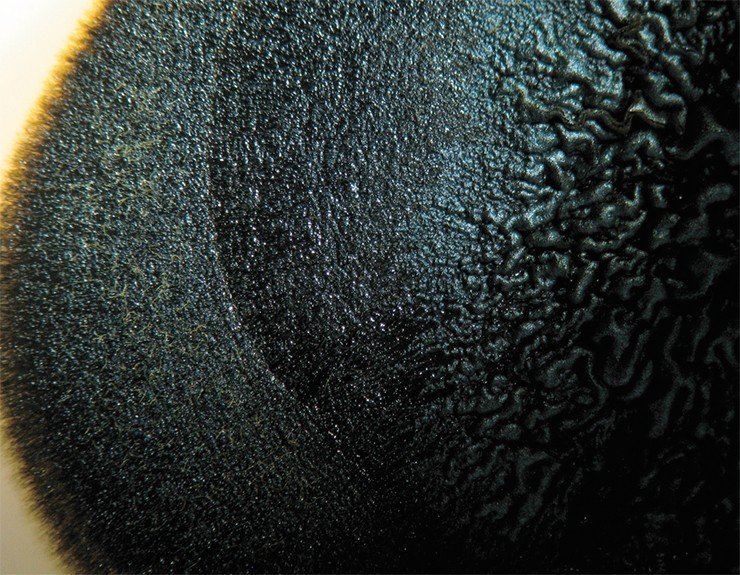
Симптомы болезни и морфология возбудителя. Признаки болезни более отчетливо проявляются в период восковой спелости зерна. У больных растений колосковые пленки несколько растопырены, и из них виден головневый мешочек [рис. 1а и б]. При раздавливании колоска из него выделяется сероватая жидкость или темная сажистая масса. Пораженные колосья легковесные, не поникают, имеют серовато-фиолетовый оттенок, издают селедочный запах, что обусловлено наличием триметиламина в составе телиоспор. При уборке пшеницы головневые мешочки разрушаются и происходит распыление телиоспор, которые оседают на зерне, стерне и почве. T. caries и T. levis различаются по морфологии телиоспор. У T. levis они светло-коричневые, гладкие, эллипсоидальные или продолговатые, округлые 18,5 × 14,5-16,6 мкм в диаметре, а у T. caries – шаровидные или слегка овальные, темно-коричневые, имеют сетчатые утолщения, образующие 5-угольные петли. T. levis наиболее вирулентен, поражает почти все виды пшеницы. Установлено, что он дифференцируется на физиологические расы, специализированные на определенные сорта (Ульянищев, 1968).
Рисунок 1. Колосья пшеницы, пораженные твердой головней (а), телиоспоры гриба Tilletia caries (б)
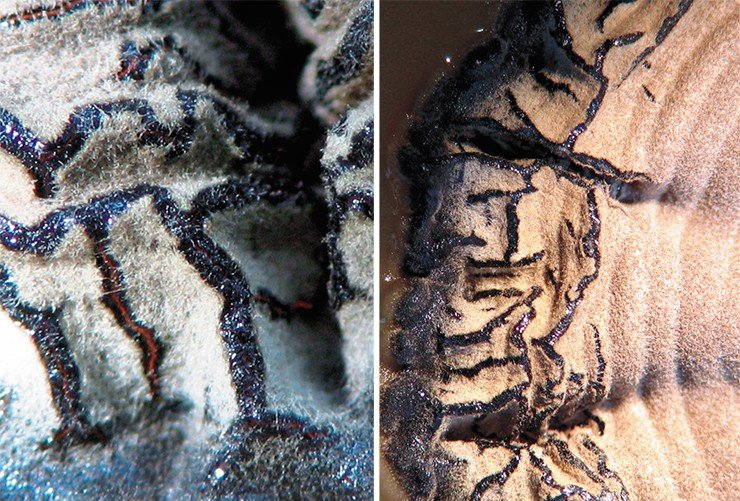
Основным источником инфекции твердой головни пшеницы являются семена, которые заспоряются во время уборки. В условиях Центральной Азии с засушливым климатом возбудитель болезни сохраняет жизнеспособность и в почве. Вместе с высеянными семенами прорастают и споры головни, образуя одноклеточные базидии с верхушечными базидиоспорами [рис. 2a и 2б]. Последние попарно копулируют и дают начало инфекционной гифе, проникающей в колеоптиле пшеницы. Далее гриб развивается диффузно, достигает конуса нарастания, у зараженных растений вместо зерен в колосе образуются головневые мешочки, покрытые сверху пленками (Шварцман, 1960).
Распространение и вредоносность. Твердая головня широко распространена во всех регионах Центральной Азии, в южном и юго-восточном Казахстане, где в основном возделывают озимую пшеницу, а также в восточном. В северном и западном регионах на яровой пшенице она встречается крайне редко. Широкое внедрение почвозащитной технологии возделывания этой культуры, для более эффективного использования июльских осадков перенесение сроков её посева на вторую половину мая, нарушило установившуюся взаимосвязь между возбудителем болезни и растением-хозяином.
Как известно, оптимальная температура для прорастания спор гриба T. caries и заражения ими пшеницы находится в пределах 8-13°С (Ишпайкина с соав., 1972). В северном регионе республики почва на глубине заделки семян во второй и третьей декадах мая прогревается до 15-20°С и более, что способствует быстрому и дружному прорастанию семян и уходу проростков от заражения патогеном.
В 90-е годы прошлого столетия в южном, юго-восточном и восточном регионах Казахстана посев непротравленных семян приводил к резкому увеличению пораженности озимой пшеницы твердой и карликовой головней. Так, фитоэкспертиза семян, засыпанных под урожай 1994 г. в Саркандском районе Алматинской области показала, что 21,9% не кондиционны по зараженности инфекцией головни. Заспоренность их достигала 15-20 тыс. спор на 1 зерно, что в сотни раз превышало допустимый уровень. В ПК«Пограничник» 2 000 тонн семян элиты сорта Богарная 56 были не пригодны для посева и пищевых целей. В 1997-1998 гг. в отдельных хозяйствах южного и юго-восточного регионов Казахстана убранное зерно озимой пшеницы непригодно для переработки на муку и корм животным, т.к. содержит высокотоксичное вещество со специфическим запахом. Пораженность колосьев твердой и карликовой головней достигала 15-38%, т.е. только от одной болезни допущены потери 1/3 части урожая (Койшыбаев, 1995; 2002).
Карликовая головня
Возбудитель болезни – гриб Tilletia controversa Kuehn., состоит из двух физиологических форм: T. controversa f. sp. tritici поражает только озимую пшеницу и T. controversa f. sp. agropyri – пырей ползучий.
Симптомы болезни и морфология возбудителя. Отличается от твердой головни по характеру проявления болезни, морфологии телиоспор и биологическим особенностям возбудителя. Пораженные карликовой головней растения сильно кустятся (от 4 до 50 шт.) и заметно отстают в росте, колос становится ветвистым, в колосках образуются до 6-7 округлых, глубоко расположенных головневых мешочков. Телиоспоры T. controversa более крупные (21,2-20,4 мкм), хорошо выраженной сетчатой оболочкой, высотой ребра 1,5-4 мкм [рис. 2а и б], прорастают после дозревания при температуре от +2-3 до 10-15°С, влажности почвы от 15 до 60%, сохраняют жизнеспособность в почве до 5-7 лет (Шварцман,1960; Ульянищев, 1968).
Рисунок 2. Прорастание телиоспор у головневых грибов: семейства Ustilaginiaceae (а), Tilletiaceae (б)
Распространение и вредоносность. Заболевание распространено в Центральной Азии и Закавказье на видах пырея (Agropyrum) и волоснеце (Elymus multicatulis), при искусственном заражении поражает пшеницу – Tilletiа aestivum и T. сarthlicum. Наиболее вредоносная болезнь озимой пшеницы. В Казахстане впервые была обнаружена в начале 60-х годов прошлого столетия, в предгорной и горной зонах, расположенных на высоте 800-1 000 м и более над уровнем моря. В 1971 г. в Саркандском районе обнаружена на площади 3 656 га с распространением 18%, сорт Мироновская 808 на 28 га был поражен ею на 70%, а Безостая 1-27%. В 1987 г. в бывшей Талдыкорганской области заболевание было выявлено на 30,7% обследованной площади, а в отдельных хозяйствах количество пораженных им колосьев в посевах достигало 13%. Анализ динамики карликовой головни на озимой пшенице на Саркандском сортоучастке в период 1988-2000 гг. показал, что заметное её проявление (до 10-15%) отмечалось в 1991, 1992, 1995-1997 и 2000 гг. что, связано с оптимальными условиями погоды в период посев-всходы (Койшыбаев, 2002). Как известно, успешное заражение озимой пшеницы возбудителем болезни происходит при низкой температуре почвы (4-6°С). В Кыргызстане карликовая головня распространена на Ферганском хребте на высоте 900-1 200 м над уровнем моря, пораженность колосьев озимой пшеницы достигала 10-15%. В Ошской области из обследованных в 1988 г. заболевание выявлено на 49% площади (Кошеляева, 1992).
Пыльная головня
Возбудитель болезни – гриб Ustilago tritici (Pers.) Yensen.
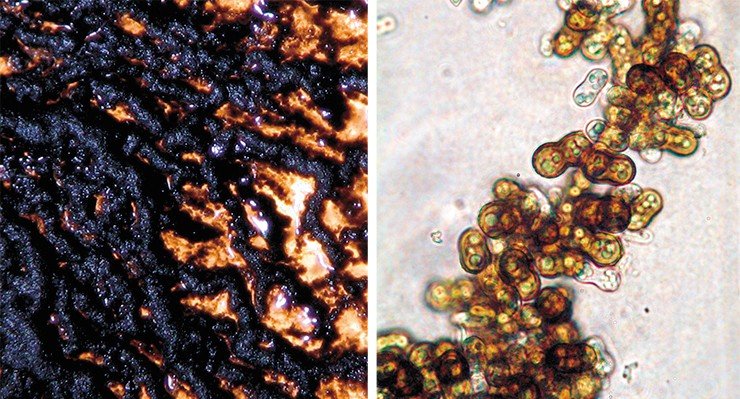
Симптом болезни, морфологические и биологические особенности возбудителя. Все органы колоса, за исключением стержня, до выхода из влагалища верхних листьев, полностью превращаются в черную, сажистую массу [рис. 3а], состоящую из телиоспор гриба [рис. 3б]. По форме они шаровидные, эллипсоидальные, иногда угловатые светло-оливковые или коричневые, с одной стороны слегка утолщенные, с другой – прикрытой, маленькими бородавочками, оболочкой; размер их колеблется в зависимости от зоны возделывания и часто составляет 7-9 × 5-7 мкм.
В период цветения пшеницы происходит интенсивное распыление телиоспор, они попадают на рыльце завязи, где прорастают в промицелий [рис. 3б]. В результате слияния 2-х его клеток образуется инфекционная гифа, которая проникает через пыльцевую трубку в завязь. Грибницу возбудителя можно обнаружить в различных тканях семян: плодовой оболочке, щитке, зародыше и зачаточном корешке. Зараженные мицелием пыльной головни семена внешне не отличаются от здоровых. Она сохраняется в состоянии покоя до следующего года и когда высеянные в почву семена прорастают, трогается в рост и возбудитель болезни. Развиваясь диффузно, мицелий достигает зачаточного колоса, где сильно разрастается, утолщается, ослизняется и распадается на хламидоспоры, полностью уничтожая колос. В отдельных случаях, поражается болезнью только нижняя его часть, на верхней – формируется зерно. Частичное поражение колоса не является защитной реакцией растения-хозяина и не наследуется в потомстве (Шварцман, 1960; Ишпайкина с соав. ,1972).
Распространение и вредоносность. Степень поражения посевов пыльной головней зависит от особенностей цветения пшеницы, погодных условий этого периода, а также устойчивости сорта. Прорастание телиоспор гриба и заражение растений происходят только при наличии капельно-жидкой влаги или при влажности воздуха 60-70%, температуре – 20-25°С. Заметное проявление болезни наблюдается в северном и северо-восточном регионах Казахстана, где в период колошения-цветения пшеницы часто выпадают осадки, среднесуточная влажность воздуха достигает 65-75%. Установлено, что характер цветения пшеницы и его продолжительность, длительность пребывания цветка в открытом состоянии существенно влияют на поражаемость сорта (Пенчукова, 1974).
Рисунок 3. Пыльная головня пшеницы (а), телиоспоры Ustilago tritici (Pers.) Yensen (б)
В связи с широким внедрением системных препаратов из групп карбоксина, карбендазима и триазолов для протравливания семян заметно сократились пораженные пыльной головней площади и снизилось её распространение. В начале 90-х годов в Казахстане она обнаружена только на 7,6% апробированной площади со средним количеством больных колосьев 0,1-0,01%, максимальным – 1,6%.
При мониторинге посевов озимой пшеницы в период 2001-2005 гг. и 2012-2014 гг. в южном и юго-восточном регионах она не обнаружена, а в северном регионе на яровой пшенице она встречалась крайне редко, количество пораженных колосьев не превышало 0,1-0,01%, т.е. было очень низкое.
Индийская (карнальская) головня
Возбудитель болезни – гриб Tilletia indica (син.: Neovossia indica Mand.).
Заболевание является эндемичным для субконтинента Азия; впервые обнаружено в Индии в 1936 году, затем распространилось в Афганистан, Пакистан и Непал. Позже его завезли семенами в Мексику, где патоген успешно акклиматизировался. Является карантинным объектом для республик Центральной Азии. По симптомам проявления она заметно отличается от других видов головни.
Характерный признак болезни – черная сажистая споровая масса, образующаяся на бороздке зерна под эпидермисом, часто на зародышевой его части. Поражаются отдельные зерновки на колосе, заболевание заметно в период восковой и полной спелости зерна, как твердая головня, издает селедочный запах (Sing et all. 1980; 1982; Prescott et all, 1986).
Телиоспоры гриба значительно крупнее, чем у T. сaries, коричневые или темно-коричневые, шаровидные, диаметром 22-42, чаще 25-40 мкм, с темно-красноватой или коричневой сетчатой оболочкой.
Незрелые споры желтоватые, субгиалиновые, округлые, 10-28 мкм в диаметре, с тонкой светлой оболочкой. Источником инфекции служит в основном почва, где телиоспоры сохраняются длительное время; заражение пшеницы происходит в период цветения от спор, переносимых воздушным потоком. Они прорастают на поверхности цветка, образуя многочисленные базидии (до 30-50 и более) с базидиоспорами, которые дают ростковые трубочки, внедряющиеся под колосковые чешуи формирующегося зерна. Затем мицелий развивается между эндоспермой и семенной оболочкой, образует головневый сорус, состоящий из черных телиоспор. Многолетние исследования ученых Индии показали, что степень проявления болезни зависит от погодных условий периода колошение-налив зерна. Оптимальная температура для прорастания спор патогена находится в пределах 18-22°С, относительная влажность воздуха – 70-80%. Заболевание в новые регионы распространяются семенами (Sing et all, 1980) [рис. 4].
Рисунок 4. Карнальская головня пшеницы (а), телиоспоры T. indica
Карнальской головней поражаются дикие виды пшеницы: Triticum shareonensis, T. variaabilis, T. ovatum, T. scerrit, а также тритикале, рожь и близкие к ним злаки. Воздушными потоками споры могут переноситься из Афганистана в приграничные территории Узбекистана и Таджикистана, семенами в любую страну. Трудноискоренимое заболевание, инфекция его в виде телиоспор сохраняется в почве
до 5 лет. В связи с этим необходимо проводить постоянный карантинный досмотр импортируемых семян пшеницы, тритикале и озимой ржи из стран, где оно распространено. В случае проникновения болезни, искоренить её путем применения комплекса организационно-хозяйственных, агротехнических и химически приемов. Семеа обязательно протравливать одним из системных препаратов из групп беномила, пропиконазола, тиабендозола, которые высоко эффективны против головневых болезней (Prescott et all, 1986).
Стеблевая головня
Возбудитель болезни – гриб Urocystic tritici Korn, чаще поражает дикорастущие злаки, в частности пырей ползучий и мягкую пшеницу (T. aestivum). На листьях, влагалище и стеблях развиваются удлиненные черные полосы, прикрытые эпидермисом. Головневый сорус содержит округлые или эллипсоидальные клубочки телиоспор диаметром 20-45 × 12-38 мкм, состоящие из 3-5 центральных спор коричнево-бурого цвета шириной 12-16 мкм и периферических, эллипсоидальных или шаровидных, светло-желтых. Инфекция семенами не передается, сохраняется на пораженных органах растений. В южном, юго-восточном и северном регионах Казахстана встречается редко и не имеет экономического значения (Шварцман, 1960).
Ржавчинные болезни
Возбудители ржавчинных болезней – грибы, относящиеся к порядку Urediniales – облигатные организмы, т.е. рост их возможен только на живом субстрате. Цикл их развития сложный и состоит из
5 стадий, которым соответствуют столько же типов спороношения:
0 – спермогонии со спермациями;
I – эции с эциоспорами;
II – урединии с урединиоспорами;
III – телии с телиоспорами
IV – базидии сбазидиоспорами.
Если весь цикл гриба проходит на одном растении, то он называется однодомным, а на двух, относящихся к разным семействам или порядкам – двудомным или разнохозяинным. Например, у стеблевой ржавчины злаков спермации и эции развиваются на видах барбариса, урединии и телии – на злаках. Базидиальная стадия образуется на пожнивных остатках растений, где гриб зимует в виде телиоспор. Барбарис является промежуточным, а злаки – основным его хозяином (Лавров,1951; Неводовский, 1956).
Возбудители ржавчины пшеницы относятся к роду Puccinia, отличительным признаком являются 2-х клеточные, темно-бурые (в массе черные) телиоспоры, сидящие на коротких ножках. Урединиоспоры – эллипсоидальные, неправильной формы, желтой, оранжевой или бурой окраски. Виды этого рода развиваются по полному циклу,в урединио- и телиостадии паразитируют на диких и культурных
злаках, спермогониальном и эцидиальном – на двудольных растениях (барбарис, лещица, василистник и др.). Они могут развиваться и по неполному циклу, например, возбудитель желтой ржавчины –
P. triiformis сохраняется в виде урединиомицелий на озимых или дикорастущих злаках, летом развивается на яровой пшенице и ячмене.
На одном виде или роде злаков может встречаться несколько видов ржавчины, например, на пшенице – стеблевая, бурая и желтая, на ячмене – карликовая, желтая и стеблевая, на овсе – корончатая и
стеблевая. Они узкоспециализированны, отдельные виды, поражающие многие дикорастущие и культурные злаки, состоят из специализированных форм, паразитирующих на одном или нескольких видах
растений, которые в свою очередь распадаются на физиологические расы или биотипы, приспособленные к определенным сортам.
После проникновения в ткань растения гриб развивается в межклетниках, высасывая питательные вещества из клеток хозяина с помощью гаусторий. Под эпидермисом листьев на коротких ножках, отходящие от грибницы, образуются многочисленные урединио- и телиоспоры, которые при созревании разрывают эпидермис и разносятся воздушным потоком. Заболевание, как правило, проявляется локально, только в отдельных случаях наблюдается диффузное распространение патогена по ткани. В зависимости от температуры воздуха с момента заражения до проявления болезни (инкубационный период) проходит от 5-7 до 10-15 суток. Вредоносность ржавчинных болезней заключается в том, что в результате образования некротических пятен и пустул на листьях резко снижается ассимиляционная их поверхность, из-за разрыва их эпидермиса усиливается интенсивность испарения воды. При поражении стебля ухудшается снабжение растений водой и отток запасных веществ с листьев на репродуктивные органы. Все это приводит к снижению урожая и качества зерна.
Стеблевая (линейная или черная) ржавчина
Возбудитель болезни – гриб Puccinia graminis Pers., состоит из нескольких специализированных форм: P. graminis f. sp. tritici поражает пшеницу, ржаная f. sp. secalis – рожь и ячмень.
Симптомы болезни, цикл развития и биологические особенности патогена, пути сохранения и резервации инфекции. Поражаются преимущественно стебли, реже листья, колосковые пленки, где образуются крупные, оранжевые пустулы, расположенные линейными рядами. Телиоспоры зимуют на пожнивных растительных остатках, весной прорастают и образуют базидии с базидиоспорами.
Последние заражают листья и ягоды барбариса, где появляются шаровидные спермогонии со спермациями. В результате слияния последних, из различных спермогониев возникают чашевидные эции,
содержащие шаровидные и бесцветные эциоспоры. Последние разносятся ветром, заражают дикие и культурные злаки: на междоузлиях стебля, реже на листовых пластинках образуются крупные, оранжевые или кирпично-красные урединиопустулы, располагающиеся линейными рядами [рис. 5а]. Урединиоспоры имеют продолговатую форму, шиповато-бородавчатую оболочку, желтовато-бурые, овальные, размером 21-35×12-20 мкм. К концу вегетации пшеницы пустулы становятся почти чёрными, блестящими, что свидетельствует о наступлении телиостадии гриба. Телиоспоры 2-х клеточные, веретеновидные или булавовидные, с гладкой оболочкой, сильно утолщенной, темно-бурой верхушкой, размером 27-77 × 13-22 мкм [рис. 5б].
Еще в 1913 году Е. Стэкман установил, что барбарис является промежуточным хозяином возбудителя стеблевой ржавчины пшеницы, анализировал эволюцию рас патогена в США. Многие исследователи изучали биологические его особенности, специализацию, пути сохранения и резервации инфекции в природных условиях. Н.Н. Лавров (1951) на основе многолетних исследований и наблюдений сделал вывод, что в условиях Западной Сибири барбарис не играет особой роли в жизненном цикле гриба, и возбудитель перезимовывает в урединиостадии в тканях многолетних злаков, в частности пырея ползучего (Agropyron repens).
Рисунок 5. Стеблевая ржавчина пшеницы (а) и её телиоспоры (б)
В Казахстане гриб P. graminis развивается в спермогониальной стадии на видах барбариса (Berberis vulgaris и др.), урединии – на пшенице, а также на других культурных и дикорастущих злаках (Неводовский, 1956). В то же время исследования В.В. Плахотника (1974) показали, что в лесах и парках Северного Казахстана произрастает около 600 кустов барбариса, на которых развивается ржаная форма гриба, а пшеничная встречается крайне редко. В опыте с искусственным заражением 13 видов злаков пшеница поражалась только мятликовой формой. Резерваторами инфекции могут служить многолетние культурные и дикорастущие злаки из трибы ячменных, в частности виды пырея (Agropyrum repens, A. ramosum), волоснеца (Elymys multikaulis, E. junceus, E. sibiricus) и житняка (A. tenerun, A. cristatum, A. pectiniforme).
Выживаемость урединиоспор гриба зависит от условий послеуборочного периода. При сухой осени и мягкой зиме возбудитель сохраняет жизнеспособность до июня, однако частые осадки в октябре и ноябре в сочетании с теплыми днями для него губительны.
В.П. Турапин и В.А. Мостовой (1995) считают, что в Северном Казахстане барбарис и дикие злаки не являются резерваторами инфекции стеблевой ржавчины пшеницы и эпифитотии болезни в основном обусловливаются заносом спор из сопредельных стран ближнего и дальнего зарубежья. В 1981 и 1986 гг. развитие болезни на ней не превышало 5-10%, при пораженности ею дикорастущих злаков на 50-100%. Она на яровой пшенице обычно проявляется в начале августа от инфекции, заносимой из Западной Сибири. При наличии капельно-жидкой влаги или высокой относительной влажности воздуха (90-100%) урединиоспоры прорастают через 2 часа. При оптимальной температуре (25°С) инкубационный период болезни составляет 7-9 суток. Они устойчивы к низким отрицательным температурам, под глубоким слоем снега сохраняют жизнеспособность на стерне.
Наши наблюдения в 1996-2000 гг. в дендропарке возле поселка Шортанды (Акмолинская обл.) показали, что на барбарисе во второй и третьей декадах мая развиваются спермогонии и эции стеблевой ржавчины. В 1999 г., несмотря на слабое её развитие на промежуточном хозяине, сильно поразился ею волоснец ситниковый (до 50-75%). В 2000 г. в начале первой декады июня её урединиопустулы обнаружены на мятлике луговом. В результате благоприятных условий, сложившихся в июне (выпало 62 мм осадков, средняя относительная влажность воздуха в пределах 68-73%), наблюдалось эпифитотийное развитие болезни на многих дикорастущих и культурных злаках. Анализ во второй декаде июля показал, что наиболее сильно (до 75-100%) поразились ею мятлик луговой, ячмень дикий (или собачий), житняк ширококолосый, волоснец ситниковый, пырей бескорневищный, несколько слабее – житняк узкоколосый; заболевание не проявилось на костре безостом и костреце, которые росли рядом. Многолетние злаковые травы, посеянные на расстоянии до 10-15 км от промежуточного хозяина, сильно поразились стеблевой ржавчиной. На ячмене выявлены единичные её пустулы, на пшенице заболевание не проявлялось, несмотря на то, что посевы житняка, находящиеся на расстоянии 50-100 метров поразились стеблевой ржавчиной в сильной степени. Полученные данные свидетельствуют о том, что на барбарисе развивалась не пшеничная форма, а мятликовая – P. graminis f. sp. poa [табл. 2].
В 2003 г. в РГКП «Заречное» (Костанайская обл.) озимая рожь была поражена стеблевой ржавчиной в начале налива зерна (I декада июля) до 10-25%, единичные урединии обнаружены на житняке и нижних междоузлиях яровой пшеницы. Слабое её проявление на последней культуре дает основание считать, что на озимой ржи паразитировала f. sp. secalis, которая поражает и ячмень: распространение болезни на нем колебалось от 20 до 50%, степень пораженности – до 10-25%. На Карабалыкской опытной станции на озимой пшенице наблюдали слабое проявление стеблевой ржавчины, на яровой заболевание не выявлено. В 2005 г. она заметно развивалась на пырее ползучем, растущем на обочинах полей и лесопосадках, а также на житняке; на яровой пшенице первые её признаки были обнаружены в начале июля: в период трубкования – флаг листа происходило умеренное развитие. В Северном Казахстана возможна перезимовка возбудителя стеблевой ржавчины на озимой пшенице, которая высевается в основном для экспериментальных целей. Так, в 2007 г. на Карабалыкской СХОС в период трубкования-колошения (конец июня) обнаружены на ней пустулы гриба, в середине июля ею сильно поразились сорта яровой пшеницы, посеянные в питомнике конкурсного испытания. Инфекция распространялась от первоначального очага до 10-15 км (Койшыбаев, 2010).
Таблица 2. Степень пораженности стеблевой ржавчиной альтернативного хозяина, дикорастущих и культурных злаков (Акмолинская обл.)
В Западной Сибири из-за отсутствия промежуточного хозяина стеблевая ржавчина развивается по сокращенному циклу: зимует урединиомицелий на многолетних дикорастущих злаках. Пшеничная или ржаная форма переходит на яровую пшеницу, где циркулируют в урединиостадии (Чулкина с соавт., 1981).
Среднеазиатский НИИ фитопатологии (САНИИФ) проводил исследования для определения возможности заноса спор ржавчины воздушными потоками. В 1981-1986 гг. с помощью прибора ПАРЗ-1,
монтированного под фюзеляжем самолета АН-2, определяли наличие спор ржавчины в приземном слое воздуха на высоте от 100 до 3 500 м. Установлено, что концентрация спор заметно варьируется по годам и месяцам. Наибольшее их количество в воздухе зарегистрировано в северном регионе Казахстана в 1983 и 1987 гг., плотность их достигала 54-794 шт/м3. В 1990 г. над территорией Западно-Казахстанской и Оренбургской областей обнаружены споры бурой и стеблевой ржавчины на высоте от 500 до 2 500 м с концентрацией от 3-5 до 50-90 шт/м3 (Мостовой, Бережнова, 1985; Мостовой с соавт., 1988).
Распространение, многолетняя динамика и вредоносность болезни. В период 1920-1930 гг. в США происходили 4 эпифитотии стеблевой ржавчины, в 1931-1940 гг. – 2, 1951-1960 гг. – 2. Особенно опустошительными они были в 1935, 1953 и 1954 гг., катастрофически снизив урожай пшеницы. В последние 50 лет в странах Северной и Южной Америки, Западной Европы, Центральной и Южной Азии заметное развитие болезни не отмечено, за исключением Китая, Австралии и Северной Африки. В 1999, 2013 и 2014 гг. происходили эпифитотии стеблевой ржавчины в горных районах Эфиопии, в 2008 г. в Кении на необработанных фунгицидом полях урожай пшеницы снижался до 60-70% (Hodson, 2015; Patpour, 2015).
В Зауралье России эпифитотийное развитие стеблевой ржавчины происходило в 1967-1969 гг., в последние 40 лет в отдельные годы очажное развитие болезни в конце вегетации пшеницы (Немченко, 2011). В 2003-2005 гг. она проявлялась заметно в Приволжском и Западно-Сибирском агроклиматических регионах, в 2007 г. – в лесостепной зоне последнего, совместно с желтой ржавчиной (Санин с соавт., 2007).
Стеблевая ржавчина в Казахстане распространена в лесостепной и степной зонах северного региона. В 1962 г. происходило заметное развитие этой болезни на яровой пшенице в Северо-Казахстанской и Кокшетауской областях. В 1964 г. при эпифитотии болезни пораженность пшеницы в северном регионе достигала 50-60%, потери урожая составляли – от 20-30 до 50% и более. В 1967 г. на площади около 5-6 млн. га происходило сильное развитие стеблевой и листовой ржавчины, урожайность коммерческих сортов Саратовская 29, Безенчукская 98, Костанайская 14, Жана-Кызыл и других снизилась на 50,8-65,4% (Джиембаев с соавт., 1974).
В последние 50 лет в северном и других регионах республики не наблюдали заметное развитие стеблевой ржавчины на пшенице, несмотря на благоприятные погодные условия в отдельные годы. Она развивалась на диких злаках: так, в 1978-1980 гг. в пустынно-степной и предгорной зонах Алматинской области сильно поражался ею костер японский, растущий в посевах и вокруг них, на озимой пшенице она не выявлена. При мониторинге фитосанитарного состояния зерновых культур в 1998-2004 гг. в южном и юго-восточном регионах Казахстана в Чуйской и Иссык-кульской долинах Кыргызстана на озимой пшенице стеблевая ржавчина не обнаружена, в отдельные годы она заметно поражалась желтой и листовой. В 2000 г. в предгорной зоне Жамбылской области заметно поразилась стеблевой ржавчиной падалица озимой ржи.
В 1999-2000 гг. в Акмолинской области погодные условия были благоприятны и происходило сильное развитие на яровой пшенице листовой ржавчины, стеблевая не обнаружена, в Костанайской области она развивалась от слабой до умеренной степени. В 2001 г. на Карабалыкской опытной станции в фазу восковой спелости зерна пораженность коммерческих сортов не превышала 5-10%.
В 2000 и 2002 гг. в Костанайской области происходило заметное распространение стеблевой ржавчины на озимой пшенице, яровая пшеница поразилась до 10-25%. В 2006 г. в Северо-Казахстанской области она обнаружена в основном на поздних её сроках посева, пораженность стеблей не превышала 5-10%. Низкая ночная температура (8-10°С) в конце июля и в первой половине августа сдерживала её развитие, повышение её в третьей декаде месяца способствовало более интенсивному распространению болезни. В степной и лесостепной зонах оно варьировало от 20-40 до 90-100%, степень пораженности стеблей не превышала 5-10%, только в редких случаях достигала 20%. В 2007 г. в Костанайской области первые ее пустулы на озимой пшенице обнаружены в начале 2 декады июля – в период молочной и молочно-восковой спелости зерна. Распространение болезни не превышало 5-10%, пораженность стеблей – 10-25%. В горно-сопочной зоне Акмолинской области посевы озимой пшеницы ТОО «Есиль-агро» были поражены бурой ржавчиной в сильной степени, встречались единичные пустулы стеблевой, заметное её развитие наблюдали на озимой ржи.
На Карабалыкской СХОС в питомнике конкурсного сортоиспытания яровой пшеницы, удаленного от посевов озимой на 0,5-1 км, происходило сильное развитие (до 50-100%) стеблевой ржавчины.
На производственных посевах, удаленных от очага инфекции на 10-15 км, развитие болезни было слабое (1-5%) или умеренное (10-25%). В 2008 г. в Северо-Казахстанской области стеблевая ржавчина более интенсивно развивалась на среднепоздних сортах яровой пшеницы: Омская 19 и Шортандинская 95, особенно на сроках посева 25 и 30 мая (Койшыбаев, 2000; 2010).
В 2014 и 2015 гг. в Северо-Казахстанской области стеблевая ржавчина проявлялась в период молочно-восковой и восковой спелости зерна, в основном на позднеспелых сортах, степень пораженности их не превышал 10-20%, а в 2016 г. она обнаружена в начале налива зерна и коммерческие сорта поразились ею на 40-60% и более. Инфекция болезни, на наш взгляд, была занесена воздушными потоками из Западной Сибири, где на посевах озимой и яровой пшеницы заболевание в последние годы проявляется заметно (Шаманин с соавт., 2010).
Исследованиями ученых установлена возможность заноса воздушными потоками инфекции видов ржавчины из одной страны или континента в другой. Для переноса спор на дальние расстояния, прежде всего, важно направление ветра и турбулентность воздуха. Чередование сухого и влажного воздуха благоприятны для заражения, массового образования и высвобождения спор из соруса. Споры стеблевой ржавчины из Южной Африки распространяются в Западную, более высокая вероятность заноса инфекции из Эритерии в Йемен и Уганду, из Египта в Судан. Возможно распространение спор стеблевой ржавчины из Ирана в Афганистан, Пакистан и Индию. Так происходило распространение расы Ug 99 из Кении в Эфиопию, далее в Йемен и Иран (Meyer, 2015).
Вредоносность стеблевой ржавчины зависит от сроков заражения растений и интенсивности развития болезни. При эпифитотии, наблюдавшейся в 1967 г., урожай восприимчивых к стеблевой и бурой ржавчине сортов Жана-Кызыл, Кустанайская 14 и других снижался до 50-70% (Джиембаев, 1972). При инокуляции яровой пшеницы стеблевой ржавчиной в период трубкования, к восковой спелости зерна интенсивность ее развития достигала 60%, потери урожая – 39,4%, в фазу колошения – 27,3%, в период цветения и молочной спелости зерна – на 18,8% соответственно. Ухудшается качество зерна: уменьшается содержание крахмала, моно- и дисахаров, общего и белкового азота, увеличивается – небелкового азота (Мостовой, 1975; Турапин, 1986).
В 2001 г. на фоне искусственного заражения определяли вредоносность стеблевой и листовой ржавчины яровой пшеницы в Акмолинской области. В связи с особо благоприятными условиями погоды в фазе восковой спелости зерна пораженность листьев и стеблей двумя видами ржавчины достигала 75-100%, продолжительность паразитирования грибов составляла 50-60 суток, потери зерна достигали 50-60%. Масса 1 000 зерен снижалась более чем в 2 раза: у искусственно зараженных растений она не превышала 20-25 г, контрольных – 48-50 г.
В 2008 году в Северо-Казахстанской области на позднеспелых сортах и поздних сроках посева яровой пшеницы заметно проявилась стеблевая ржавчина. Анализ структуры урожая у сорта Омской-19 показал, что при средней пораженности стеблей (20-40%), масса зерна с колоса снижается до 3,2, 1 000 зерен – 6,9%, а в сильной степени – на 24,4 и 23,1% соответственно. У среднераннего сорта Памяти Азиева при пораженности стеблей на 10-25% потери урожая не превышали 4 – 6,4%, а при 50% – 13,3% [табл. 3].
В 2016 г. на Северо- Казахстанской СХОС несмотря на позднее проявление стеблевой ржавчины происходило интенсивное развитие болезни, особенно на поздних сроках посева пшеницы, заметное снижение не только урожайности, но и качества зерна. Например, у сорта Астана 2 при посеве 20 мая уровень пораженности болезнью составил 14,2%, 30 мая – 50%, масса 1 000 зерен – 27 и 19,7, натура – 643 и 592 г, у Омской 35 – 5,2 и 27,8%, 28,2 и 26,9, 602 и 577 г, соответственно.
Таблица 3. Вредоносность стеблевой ржавчины на яровой пшенице (Северо-Казахстанская СХОС, 2008 г.)
Бурая (листовая) ржавчина
Возбудитель болезни – гриб Puссinia recondita Desm. (син. – Puccinia tritici Eriks.).
Симптомы болезни, биологические особенности патогена, источники инфекции. Проявляется преимущественно на нижней стороне листьев в виде округлых, мелких, охряно-бурых пустул, содержащих бурые урединиоспоры. Они одноклеточные, округлой или эллипсоидальной формы, с буроватой оболочкой, мелкими шиповидными бородавочками, размером 20-28 мкм [рис. 6а и б]. К концу вегетации растений на нижней стороне листьев образуются блестящие черные пустулы, содержащие продолговато-булавовидные, 2-клеточные, с более утолщенной светло-бурой верхней клеткой телиоспор.
В северном регионе Казахстана эцидиальная стадия возбудителя бурой ржавчины развивается на василистнике (Thalictrum fumarioides L. Rehb.), растущем, в посевах примыкающих к березовым колкам (Эльчибаев, 1972).
Рисунок 6. Листовая ржавчина пшеницы (а), урединиоспоры гриба P. recondita (б)
Она на озимой пшенице может развиваться по неполному циклу, возбудитель перезимовывает в виде урединиомицелий на её всходах, проявляется рано, затем переходит на яровую пшеницу. За лето гриб дает несколько урединиогенераций, которые способствуют распространению патогена. В районах, где одновременно возделывают озимую и яровую пшеницу, вероятность возникновения эпифитотии болезни больше и вредоносность выше.
Встречаются 2 специализированные формы возбудителя бурой ржавчины: P. tritici f. thalictri и P. tritici f. isopyri. В условиях Западной Сибири на видах василистника: Thalictrum minus, Th. flavum и Th. simplex. паразитирует не пшеничная форма P. recondita. На прилегающих к ней территориях Северного Казахстана широко распространена лещица (Isopyrum fumarioides), которая в основном произрастает на
залежах, вдоль дорог и вспаханных землях. В.А. Брызгалова (1955) впервые установила, что она является промежуточным хозяином возбудителя бурой ржавчины пшеницы (Гешеле, 1956).
Возбудитель болезни развивается при температуре от 6 до 35°С, относительной влажности воздуха от 63 до 77%. При температуре 21°С его споруляция отмечается на 6 сутки, 16°С – 10 сутки, при 30- 38°С жизнеспособность урединиоспор сохраняется до трех месяцев. Осенью на отмирающих листьях пшеницы формируются телии с телиоспорами, которые хорошо переносят низкие температуры (до −30-40°С). Весной они прорастают в базидию с базидиоспорами, которые заражают промежуточного хозяина – василистника или лещицу. Урединиоспоры гриба прорастают в капельно-жидкой влаге при 18-25°С через 2-3 ч и дают ростки, которые через эпидермис листа проникают в межклетники. Для заражения растений достаточно кратковременного дождя или росы. При среднесуточной температуре 20-25°С продолжительность инкубационного периода болезни составляет 6-7 суток, при 15-18°С удлиняется до 10 суток (Гешеле,1955; Приходько, 1981; (Эльчибаев,1972; Турапин, Эльчибаев, 1972, 1981).
Резерваторами инфекции бурой ржавчины могут быть многие дикорастущие злаки. При инокуляции урединиоспорами гриба, собранными с пшеницы, поражались ими некоторые виды волоснеца (Elymus gigantheus Vahl., E. Junceus Fisch., E. рavonus Claus.), житняк ширококолосый, регнерия омская, эгилопс Крапса, ячмень и озимая рожь.
С.С. Санин (2007) указывает, что в европейской части Российской Федерации основной источник инфекции – пораженные посевы озимой пшеницы и её падалицы, где возбудитель перезимовывает и весной возобновляет свое развитие, а также дикорастущие злаки и споры, переносимые воздушными потоками. Оптимальная температура для заражения растений 15-20°С и сохранение капельно-жидкой влаги не менее 4-5 часов.
А.А. Эльчибаев (1972) считает, что в Северном Казахстане лещица дымянковидная (L. fumarioides L.) не имеет широкого распространения, на лугах и березовых колках растет василистник простой (T. simplex). При инокуляции пшеницы эциоспорами из василистника на 8 день обнаруживались единичные урединии гриба (до 1%). Однако в полевых условиях не всегда удавалось заразить эциоспорами
с промежуточного хозяина пшеницу.
По данным В.П. Турапина и В.А. Мостового (1995), василистник не имеет особой роли в резервации и передаче инфекции бурой ржавчины на пшеницу. В июне и первой половине июля на поймах рек Ишима и Тобола, а также в лесных колках происходило развитие эции ржавчины на промежуточном хозяине, однако заболевание не проявилось на яровой пшенице. Авторы считают, что потенциальными резерваторами инфекции являются культурные и дикие злаки, в частности виды житняка, волоснец ситниковый и гигантский, пырей бескорневищный, ячмень, рожь озимая. В то же время, при многократной инокуляции пшеничной формой P. recondita многих дикорастущих злаков на их листьях образовывались только хлоротичные пятна и некрозы, что свидетельствует об узкой специализации возбудителя болезни.
Многолетние наблюдения в северном регионе показали, что дикорастущие злаки и промежуточные хозяева не играют особой роли в циркуляции патогена. Так, в 2000 и 2001 гг. в Акмолинской области происходило эпифитотийное её развитие на яровой пшенице, коммерческие её сорта поразились до 50-100%. Однако заболевание не проявлялось на житняке, пырее бескорневищном, волоснеце ситниковом, костре безостом, за исключением кострицы, на которой заболевание проявилось в умеренной степени (Койшыбаев 2000; 2012).
В резервации возбудителя бурой ржавчины в западном, северном и восточном регионах Казахстана определенное значение имеет озимая пшеница. Возможна перезимовка патогена в виде урединиомицелий на её всходах и раннее возобновление болезни. Исследования в Уральской области в 1986-1990 гг. показали, что пораженность её всходов осенью составляла 80-100%, отрастающих
растений весной 15%. При благоприятных погодных условиях распространение болезни на озимой пшенице в конце мая и начале июня достигало 90-100%, степень пораженности листьев от 20-30% до 80-100% (Турапин, Мостовой, 1995).
В северном регионе озимая пшеница возделывается для опытных целей на ограниченной площади. Её сеют во второй и третьей декадах августа, и с осени всходы поражаются ржавчиной; патоген перезимовывает в виде урединиомицелий, весной происходит раннее возобновление болезни и распространение на яровую пшеницу. Так, в 1992 г. в ОПХ «Заречное» Костанайского НИИСХ осенью всходы озимой пшеницы поразились бурой ржавчиной до 90-100%: в период молочно-восковой спелости зерна (первая декада июля) пораженность её листьев болезнью достигала 25-50%, инфекция распространялась на яровую пшеницу. Установлена определенная зависимость в степени поражения её посевов от удаленности источника резервации патогена. Яровая пшеница, размещенная на расстоянии 100-200 метров от озимой, поражалась бурой ржавчиной на 10-25%, на 2-3 км – 1-5%. В 2002 г. наблюдали раннее проявление листовой ржавчины на озимой пшенице, эпифитотийное её развитие – на яровой. В 2003 г. на первой культуре происходило слабое развитие болезни, на второй – очень сильное. В 2005 г. из-за зимних морозов озимая пшеница вымерзла, несмотря на это, происходило сильное развитие болезни на яровой пшенице в северном регионе на огромной территории, что свидетельствует о заносе инфекции воздушными потоками.
В 2007 г. в горно-сопочной зоне Акмолинской области в начале налива зерна посевы озимой пшеницы ТОО «Есиль-агро» были поражены бурой ржавчиной до 50-100%. На яровой пшенице, размещенной от озимой на расстоянии 5-6 км, пораженность листьев болезнью достигала 10-25%, удаленных на 25-30 км и более – не более 1-5%.
В Западной Сибири бурая ржавчина развивается, как правило, по сокращенному, реже полному циклу. Возбудитель перезимовывает часто на озимой пшенице и многолетних злаковых травах: пырее ползучем, овсянице луговой, мятлике обыкновенном, ломколоснике ситниковом и др. Яровая пшеница заражается урединиоспорами патогена, заносимыми воздушными потоками из других регионов. Заболевание проявляется в первой и второй декадах июля, т.е. в фазу стеблевания -колошения яровой пшеницы, максимальное её развитие происходит в период молочно-восковой спелости зерна, в течение вегетации растений дает 5-8 урединиогенераций: в июле – 1-2, августе – 4-6. Продолжительность ее зависит от температуры воздуха: при 10°С – 16 суток, 15°С – 10, 20°С – 7; сильное развитие болезни наблюдается при ГТК 1,2-1,4 (Чулкина с соавт., 1987).
В.А. Мостовой с соавторами (1985; 1987) изучали пути заноса урединиоспор возбудителя бурой ржавчины по облачной системе и атмосферными осадками. Авиазондирования воздуха на высоте 3 600 м показали, что концентрация спор в июне составляла 0,1-5 шт/м3, она возрастала, в августе достигала 1 500 спор на 1 м3. В 1990 г. в Западном Казахстане на высотах 500-1 100 и 2 050-2 500 м в начале второй декады июня отмечалось до 50-90 спор P. recondita на 1 м3 воздуха. Установлено, что при наличии конвективных потоков над очагами развития болезни на высоте 1 300-2 000 м содержание спор в воздухе достигает 10-200 шт. на 1 м3, а на 1 900-3 400 м встречались уже единично. Количество спор в кучевых облаках увеличивалось до 30 раз (3-40 экз. /м3) по сравнению с подоблачным и надоблачным слоями воздуха. В Северном Казахстане в мае-июле в выпадающих осадках обнаруживалось до 37-86% спор ржавчины с концентрацией 832 тыс. шт/м3, прорастаемостью до 26,9%. Максимальное их количество (300-832 тыс. шт/м3) фиксировалось в мае-июне при очень слабом развитии бурой ржавчины на диких злаках. Установлено высокое сходство западной популяции спор возбудителя с северной, как при анализе наземной, так воздушной её популяции с высоким коэффициентом корреляции (r=0,59-0,81). В 1988 г. из 173 изолятов возбудителя болезни, собранных в приземном слое воздуха Западного Казахстана, выделен 61 патотип, в т.ч. 31 общий для обоих регионов, из 92 изолятов северного региона идентифицированы 48 патотипов, в т.ч. 25 сходных. На основе исследований сделан вывод, что воздушными потоками споры бурой ржавчины переносятся из западного региона в северный, вызывая эпифитотии болезни.
Л.А. Михайлова и Л.Г. Тырышкин указывают на возможность распространения инфекции бурой ржавчины из Северного Кавказа в соседние регионы, в частности Северный Казахстан и Западную Сибирь воздушными потоками. В период 2001-2008 гг. в Поволжском агроклиматическом регионе её эпифитотии происходило 6 раз, т.е. в 2001, 2003-2006 гг. и 2008 г., что связано в основном с увеличением доли посевов озимой пшеницы. В Нижнем Поволжье в патогенном комплексе пшеницы бурая ржавчина занимает далеко не последнее место, вызывая угрозу урожаю. В 2006-2008 гг. и 2011 и 2012 гг. пораженность посевов ею заметно возросла по сравнению с 2001- 2005 гг., составляя в среднем 20% (Маркелова с соавт., 2013). В Западной Сибири сильное развитие болезни наблюдалось в 2005 и 2007 гг., умеренное – в 2008, 2010 и 2011, слабое – 2006, 2008 и 2012 гг. В период 2000-2008 гг. в Северном Казахстане 5 раз происходило эпифитотийное развитие бурой ржавчины, т.е. в 2000, 2002, 2003, 2005, 2006; 3 раза умеренное – 2001, 2007 и 2008 гг., что примерно совпадает с Поволжским и Западно-Сибирским регионами России.
И.Г. Одинцова с соавторами (1989) считают, что европейская часть бывшего Советского Союза, Северный Казахстан и Западная Сибирь составляют по бурой ржавчине пшеницы один эпидемиологический район и популяции возбудителя в этих регионах имеет среднее и сильное сходство.
Анализ многолетней динамики бурой ржавчины в Казахстане за 1974-2000 гг. показал, что эпифитотии болезни в северном регионе не всегда связаны с заносом спор из западного. Из анализированных 27 лет в последнем регионе заметное её развитие происходило 8 раз: 1974, 1976, 1979, 1983, 1985, 1990, 1993 и 1994 гг., в Костанайской области – 14 раз, т.е. совпадало на 57,2%. В западном регионе в период 2004-2014 гг. острозасушливыми были 8 лет, т.е. неблагоприятными для развития ржавчины и заноса инфекции воздушными потоками в северный регион, более увлаженными только 2 года (Койшыбаев, 2001, 2014).
Распространение и вредоносность. Листовая ржавчина широко распространена во всех континентах и странах (Adnan, 2015). В Российской Федерации она встречается в подтаежной, предгорной и лесостепной зонах Сибири и Зауралье, наиболее интенсивно развивается в первой зоне, где ГТК составляет 1,2-1,4, сумма температур выше 10°С – 1 600-1 800°С. В северной и южной лесостепи и степи снижаются частота и интенсивность её проявления, за исключением пойм рек Иртыша и Оби (Чулкина с соавт., 1987).
С.С. Санин (2010) указывает, что в Российской Федерации бурая ржавчина в отдельные годы может охватить большие территории, при сильном развитии болезни потери могут достигать 20-30%. В период 1991-1996 гг. в Краснодарском крае она была распространена на 40-60% площадей посевов озимой пшеницы, в 2004 г. в связи с благоприятными условиями погоды происходило эпифитотийное её развитие.
По данным В.П. Шаманина (2009) в Западной Сибири продуктивность новых сортов яровой пшеницы достигает 5 тонн с 1 гектара, однако средняя урожайность не превышает 1,5-2 тонн, что связано с абиотическим стрессом или дефицитом осадков в период её вегетации, или в годы достаточного или избыточного увлажнения потерями от бурой ржавчины. В годы эпифитотийного развития этой болезни урожайность её снижается до 30%, по Омской области потери составляют около 660 млн, по региону 1 500 млн. тонн. Вредоносность бурой ржавчины зависит от сроков и степени проявления: при пораженности листьев яровой пшеницы в начале формирования-молочной спелости зерна на 10-25% потери не превышают 4,5%, в период колошения на 50-75% достигают 18,5-27,9%, в начале трубкования – 36-47,2% (Турапин,1991).
Бурая ржавчина распространена во всех регионах Казахстана, где возделывают пшеницу. В южном и юго-восточном она обычно проявляется поздно, заметно ею поражаются позднеспелые сорта озимой пшеницы. В северном и восточном регионах республики через каждые 2-3 года она развивается до эпифитотийного уровня. В северном регионе бурая ржавчина и септориоз проявляются часто совместно, превалированием той или иной болезни. Исследования в период 1999-2001 гг. в Костанайской и Северо-Казахстанской областях показали, что при их распространении в период трубкования-колошения пшеницы и сильном развитии потери урожая достигают 30-40%, в начале налива–молочной спелости зерна – 7-10%.
В 2000 г. в Костанайской области при сильном развитии бурой и умеренном – стеблевой ржавчины и септориоза на сорте Омская 18 недобор урожая достигал 31,5%, масса 1 000 зерен снижалась до 10-15%, что приводило к щуплости и снижению технологических его свойств. В Акмолинской области при умеренном развитии бурой ржавчины и септориоза на сорте Акмола 2 потери составили 14,1,
Целинная 3С – 7,4 и 22,9% [табл. 4].
В 2005 г. на Северо-Казахстанской опытной станции на 5 сортах яровой мягкой пшеницы определяли вредоносность бурой и стеблевой ржавчины по 2 срокам посева. Для защиты от болезней с воздушно-капельной инфекцией в период колошения часть посевов была обработана фунгицидом фалькон (0,5 л/га), его биологическая эффективность составляла 80-95%. Сорта мягкой пшеницы поразились первой болезнью до 75-100%, второй – 10-20%. Результаты анализа показали, что от комплекса болезней урожай зерна снижался от 7,2 до 17,2%, в том числе, за счет уменьшения массы 1 000 семян от 2,5 до 14,4: наибольшие потери происходили на сортах Астана, Омская 18 и Омская 28 [табл. 5].
Таблица 4. Вредоносность бурой ржавчины и септориоза в Северном Казахстане
Таблица 5. Вредоносность ржавчины в зависимости от сортов и сроков посева яровой пшеницы (Северо-Казахстанская СХОС, 2005 г.)
Желтая (чешуйчатая) ржавчина
Возбудитель болезни – гриб Puccinia striiformis West. (син.: Puccinia glumarum Eriks. et Henn.).
Симптомы болезни, морфологические и биологические особенности возбудителя. Поражаются листья и их влагалища, где развиваются в виде пунктирных линий и штрихов светло-оранжевые, лимонно-желтые пустулы, а также колосковые пленки, внутри которых формируются споры гриба, вследствие чего семена становятся щуплыми. Наряду с пшеницей, поражается ею и ячмень. Урединиоспоры округлые или эллипсоидальные, размером 17-30 × 15-20 мкм, с бесцветной оболочкой и шиповидными бородавочками. В конце вегетации растений развиваются черного цвета телии, содержащие телиоспоры –булавовидные, несимметричные, на коротких ножках [рис. 7а и б].
Рисунок 7. Листья пшеницы, пораженные желтой ржавчиной (а) и урединиоспоры P. glumarum (б)
Оптимальная температура для развития гриба 15-17°С, при 14-15°С урединиоспоры прорастают в течение 4-х часов, 7-10°С – через 8-9, при 18°-21°С и выше рост его замедляется, 25°С и выше не наблюдается (Абиев,1993).
В резервации желтой ржавчины в природе определенную роль играют дикорастущие злаки; при инокуляции пшеничной популяцией 20 видов дикорастущих и культурных злаков, поражались ею овес, ячмень, озимая и многолетняя рожь, житняк ширококолосый, райграс высокий, пырей корневищный, регнерия омская и тяньшанская и волоснец ситниковый; в природных условиях пырей ползучий, регнерия тяньшанская, костер безостый и вейник (Альмуратов, 1973).
Ю.Д. Зейналова (1975), проводившая исследования в горной зоне Алматинской области, утверждала, что при поражении желтой ржавчиной происходит заражение семян пшеницы, и они могут служить источником инфекции. Однако опыты в условиях теплицы и лаборатории не подтвердили передачу болезни семенами (Альмуратов, 1973; Абиев, Есенгулова, 1982).
В Центральной Азии промежуточный хозяин желтой ржавчины не выявлен, она развивается по неполному циклу: возбудитель в виде урединиомицелий перезимовывает на всходах озимой пшеницы или розетках листьев дикорастущих злаков, затем переходит на яровые культуры. За лето гриб дает несколько генераций урединиоспор, что способствует быстрому распространению инфекции (Малютина,1963; Шаварина, 1978; Хохлачева, Моргунов, 2000).
Высокогорная зона Алматинской области и прилегающая к ней Иссык-кульская долина Кыргызстана очень благоприятны для постоянной циркуляции возбудителя желтой ржавчины на озимой пшенице в урединиостадии. Из-за короткого и прохладного лета она созревает в начале сентября, когда уже появляются всходы текущего года посева, которые в отдельные годы осенью поражаются болезнью до 90-100% (Койшыбаев, 2010; 2012).
В предгорной зоне юго-восточного и южного регионов Казахстана местный источник желтой ржавчины отсутствует, так как уборка озимых проводится в июле, а посев – в октябре. Летний период характеризуется отсутствием осадков, высокой температурой (до 30-40°С) и низкой относительной влажностью воздуха, культурные и дикие злаки, за исключением тростника, выгорают. Для этой зоны большую роль имеет инфекция патогена, заносимая воздушным течением и дождевыми облаками из Узбекистана и Таджикистана с более мягкой зимой, где возможна перезимовка патогена на всходах в урединиостадии (Койшыбаев, 1999, 2012).
Недавно ученые Китая установили, что в резервации инфекции желтой ржавчины пшеницы в Западном регионе страны определенную роль в качестве промежуточного хозяина играют виды барбариса, которые часто растут рядом с её посевами, на нем развиваются спермогонии и эции гриба обычно в мае. При инокуляции пшеничной формой P. striiformis 35 его видов, образование эциоспор происходило на 23. Сравнение изолятов из пшеницы и барбариса методом молекулярных маркеров показало их идентичность (Kang, 2014).
Распространение и вредоносность. Желтая ржавчина представляет серьезную угрозу для продовольственной безопасности многих стран планеты. Она распространена на большей части территории Северной и Южной Америки и Европы, Восточной, Центральной и Южной Азии, Северной Африки, Австралии. По климатическим условиям 72% площадей посевов пшеницы подходит для её развития, стабильно проявляется на 42% (Pardey, 2014). В Афганистане потери урожая в 1964-1967 гг. достигли 50-60% (Чуприна и др., 1999). В регионе CWANА (Центральная и Восточная Азия, Северная Африка) желтая ржавчина опасная болезнь этой культуры, часто развивается до уровня эпифитотий, обусловливая огромные потери урожая. На втором международном симпозиуме по желтой ржавчине пшеницы, проходившем в 2014 г. в Турции, Ханс Браун (СИММИТ, Мексика) указал, что происходит стремительное увеличение ареала болезни, за 10 лет распространилась в Азию и Восточную Африку, появились устойчивые к высокой температуре расы патогена. При эпифитотиях этой болезни в Турции в 1991, 1999 и 2010 гг. потери были огромные; на юго-востоке страны в 2010 и 2013 гг. составили около 1 млн. тонн зерна, в 2014 г. она заметно развивалась на границе с Европой (Burak, 2014).
До 1939 г. в Австралии желтая ржавчина отсутствовала, хотя погодные условия были благоприятны для её развития. Возможно, инфекция болезни была занесена из другого континента, так как споры могут распространяться ветром на тысячи километров, сохраняют жизнеспособность в воздухе в течения нескольких недель. На 1 гектаре могут формироваться до 19 кг или биллионы спор ржавчины
(Park, 2012; 2015).
В Прикарпатском и Закарпатском регионах Украины, в предгорных зонах стран Центральной Азии желтая ржавчина проявляется периодически. В период 1940-2002 гг. в Узбекистане эпифитотии болезни повторялись 9 раз, вредоносность её варьировала от 10,4 до 67,2%. В 1999 г. сильное её развитие происходило в 7 областях, высокую к ней восприимчивость показал сорт Юна (Моргунов, Хохлачева и др.).
Эпидемии желтой ржавчины повторялись в 2001, 2003, 2005, 2009, 2010 гг., в 2013 развивалась совместно с листовой ржавчиной, фермеры использовали фунгициды на 60 млн. USD (Амонов, Sharma, 2014).
В Таджикистане погодные условия очень благоприятны для развития желтой ржавчины, пшеницу возделывают в межгорных долинах в условиях орошения и высокогорной зоне. При эпидемии болезни в 2003 году потери урожая достигли 50-60%, в 2004-2006 гг. происходило умеренное её развитие (20-40%), в 2007 и 2008 гг., несмотря на благоприятные погодные условия и высокую восприимчивость местного сорта Навруз она не проявилась. В 2009 году пораженность пшеницы желтой ржавчиной не превышала 10-20%, доминировала листовая, ею сильно поразились местные сорта Ватан, Шарора и Вахш (Rahmatov et all, 2009).
В Казахстане желтая ржавчина распространена в предгорной и горной зонах южного и юго-восточного регионов, где в основном возделывают озимую пшеницу в условиях обеспеченной богары и орошения. Уровень её распространения и развития заметно варьирует в зависимости от погодных условий мая и июня, когда происходит её колошение, цветение и налив зерна. Эпифитотийное развитие болезни происходило в 2000 и 2002 гг., умеренное – в 2003, 2006 и 2009 гг.
В 2000 г. в предгорной зоне Алматинской области многие сорта озимой пшеницы поразились ею к молочной спелости до 50-75%, колосковые пленки – до 10-25%. При мониторинге в южном и юго-восточном регионах установлено, что степень развития болезни уменьшается с запада на восток, что свидетельствует о заносе дождевыми облаками инфекции из Узбекистана. В горной зоне заболевание проявилось в период колошения, флаг-лист у сортов Стекловидная 24 и Безостая 1 было поражено до 10-25%, среднего и нижнего ярусов – до 50-75%. В Чуйской области Кыргызстана коммерческие сорта Кыял и Интенсивная поразились желтой ржавчиной в сильной степени.
В 2001 г. в связи с засушливыми условиями погоды желтая ржавчина проявилась в слабой степени (до 10-25%). Эпифитотийное развитие болезни в южном и юго-восточном регионах Казахстана происходило в 2002 г, когда в апреле и мае осадков выпало в 2-3 раза больше многолетней нормы. Первые признаки болезни в предгорной зоне Жамбылской области обнаружены в начале третьей декады апреля в период трубкования озимой пшеницы, в фазу колошения листья нижнего и среднего ярусов были поражены ею до 50-75%, флаг-лист – на 25-50%, в период молочной спелости зерна – на 80-100%. В результате преждевременного отмирания листьев и сильного поражения колосковых пленок формировалось щуплое зерно, урожай снижался до 30-40%. Аналогичная фитосанитарная обстановка складывалась на посевах пшеницы в Чуйской и Таласской долинах Кыргызстана (Койшыбаев с соавт., 2005).
В 2013 и 2014 гг. из-за острозасушливых условий погоды на озимой и яровой пшенице желтая ржавчина развивалась в очень слабой степени. Так, в 2013 г. в Южно-Казахстанской области апрель по гидротермическому режиму был благоприятным для развития этой болезни, выпало 84,5 мм осадков, среднесуточная температура не превышала 12,2-14,7°С, относительная влажность воздуха составляла 60-67%. Однако из-за отсутствия местной инфекции она проявилась только в середине второй декады мая, дальнейшее её развитие приостановлено из-за высокой температуры и низкой относительной влажности воздуха (выпало 11 мм осадков при норме 37 мм).
В северном регионе Казахстана желтая ржавчина встречается крайне редко. В 1997 г. в начале налива зерна она обнаружена на твердой пшенице в Сарколском (бывший Урицкий) районе Костанайской области, пораженность листьев не превышала 1-5%. В 2002 г. наблюдали заметное её развитие (до 10-20%) на яровой мягкой пшенице и диком ячмене в Центральном Казахстане и северном – в Акмолинской области. Лето было дождливое и прохладное, возможно, инфекция болезни была занесена воздушными потоками из южного и юго-восточного регионов, где происходило эпифитотийное развитие болезни. В Северо-Казахстанской и Костанайской областях она не обнаружена (Койшыбаев с соавт., 2005).
Желтая ржавчина также отсутствует в Зауралье и Западной Сибири, за исключением горно-лесной зоны Алтайского края (Чулкина с соавт, 1987). В 2009 – 2010 гг. в Краснодарском крае происходило эпифитотийное развитие этой болезни, что было обусловлено затяжной и холодной весной и обильными осадками (Аблова, Беспалова и др., 2011).
В горной зоне Алматинской области при пораженности листьев озимой пшеницы желтой ржавчиной в период колошения на 10%, потери урожая составили 5,3%, 25 – 16,1 и 50% – 31,7%; в начале формирования зерна – соответственно 2,9; 7,8 и 15,6%. При поражении колосьев на 50% продуктивность их снижалась на 12,7%, 75-100 – на 18-23,5%. Масса 1 000 зерен у здоровых растений составляла 43,2 г, при поражении колосьев на 50% – 31,7 г; 75-100% – 35,5-32,1 г, т.е. снижалась от 12,7 до 25,4% (Зейналова, 1977).
Если, в 1961-1999 гг. средние мировые потери урожая пшеницы от желтой ржавчины не превышали 0,5-1%, то в 2000-2012 гг. достигли 5,7% или более 1 млрд. долларов (Pardey, 2014). В 1999-2000 гг. при эпифитотийном развитии болезни в Таджикистане и Узбекистане урожай озимой пшеницы снизился до 40-50% и более. При её эпидемиях в Иране в 1993, 1995, 2010 и 2011 гг., недобор зерна составлял до
300 тыс. тонн. В некоторые годы желтой ржавчиной пшеница поражается в фазу всходов, если не обработать фунгицидом такие посевы, то потери достигают 50-75% или урожай уничтожается полностью. Эпидемия желтой ржавчины в 2010 г. в Эфиопии охватила 600 тыс. га площади этой культуры, для предотвращения огромных потерь урожая проводилась обработка посевов фунгицидами, затраты составили более 3,2 млн. долларов. В 2013 г. складывалась аналогичная ситуация, благодаря своевременному уведомлению фермеров, приняты меры для эффективного контроля болезни, потери были минимизированы и собран рекордный для страны урожай.
В 1992 и 1999 гг. в Китае эпидемией желтой ржавчины были охвачены 6,7 млн. га посевов пшеницы, в 2009 г. она сильно проявлялась в центральном и южном регионах, потери урожая достигли 20-26%, на большой площади проводилась обработка посевов фунгицидом (Chen, 2014).
Мучнистая роса
Возбудитель болезни – гриб Erysiphe graminis DС., синоним: Brumeria graminis (DC) Speer., пшеницу поражает форма f. sр. tritici March., а рожь – f. sp. secalis March.
Симптомы болезни, морфологические и биологические особенности возбудителя. Признаки болезни проявляются на листьях, междоузлиях стебля и колосковых пленках в виде белого, рыхлого мучнистого налета, состоящего из конидиеносцев и конидий гриба [рис. 8а и б]. Они бесцветные, одноклеточные, цилиндрические или бочонковидные, размером 25-40 × 8-10 мкм, образуют длинную цепочку в конце мицелий. Гриб в течение вегетации пшеницы образует несколько генераций конидиального спороношения, которые способствуют быстрому распространению болезни. Постепенно налет уплотняется, становится серым и войлочным, на грибницах появляются бурые точки – плодовые тела гриба (клейсткарпии или клейстотеции) шаровидной формы с многочисленными придаткам; в них формируется по 8-16 сумок, содержащих по 4-8 аскоспор эллипсовидной формы, размером 20-23 × 11-13 мкм [рис. 8б].
Рисунок 8. Листья и колос пшеницы, пораженные мучнистой росой (а), клейстотеции гриба (б)
В южном и юго-восточном регионах Казахстана возбудитель мучнистой росы зимует на послеуборочных остатках пшеницы (солома, колосковые пленки) в виде недозрелых клейстотециев. Весной происходит дозревание и интенсивное выбрасывание из них аскоспор и заражение растений. В Западном регионе возбудитель болезни зимует на всходах озимой пшеницы в виде мицелий, а в отдельные
годы – аскоспоры в клейстотециях. В годы, когда в сентябре и октябре выпадает много осадков (около 50-60 мм в месяц), они созревают осенью, заражают всходы озимой пшеницы, гриб зимует на листьях в виде мицелиальной подушечки, весной следующего года гриб возобновляет свое развитие и образует конидии, которые заражают листья яровой пшеницы (Доровская, Габдеев,1978). В Кыргызстане клейстотеции формируются при среднесуточной температуре до 21°С, созревание аскоспор наблюдается в августе-сентябре и они заражают всходы озимой пшеницы.
Гриб Erysiphe graminis состоит из нескольких специализированных форм: пшеничная (f. sp. tritici), ячменная (f. sp. hordei), пырейная (f. sp. аgopyri), мятликовая (f. sp. рoa) и др., которые поражают ограниченный круг злаков: пшеничная – мягкую и твердую пшеницу, эгилопс и волоснец; ячменная – ячмень заячий, луковичный и дикий (Гешеле, 1953; Васягина с соавт., 1968). Тритикале не поражается этой болезнью.
На юго-востоке Казахстана встречаются пшеничная, ячменная и пырейная формы E. graminis. При искусственном заражении первой формой гриба, кроме пшеницы, поражались эгилопс цилиндрический, волоснец ситниковый и тяньшанский, рожь озимая и многолетняя, пырей и регнерия тяньшанская. Ячменной формой поражались пырей тяньшанский, ежа сборная и эгилопс цилиндрический, пырейной – пшеница, эгилопс, волоснец ситниковый и тяньшанский, ячмень и ежа сборная (Турсумбаев, 1972).
И.М. Шаймарданов (1988) считает, что гриб E. graminis обладает широкой специализацией. В южном и западном регионах Казахстана он выявлен в сумчатой стадии на 43 видах злаков, конидиальной – 54. При искусственной инокуляции растений аскоспорами гриба в фитотроне удалось заразить 47 видов злаков, конидиями – 64, относящихся к 26 родам.
Многолетние наблюдения в предгорной зоне Алматинской области показали, что мучнистой росой не поражаются житняк, ежа сборная, костер безостый и многие виды диких злаков. Заметное её развитие происходит на пырее ползучем и мятлике луговом, с которых, вероятно, заражаются ячмень и пшеница. В северном и восточном регионах сильно поражаются мучнистой росой озимая рожь и пшеница, на их листьях происходит перезимовка патогена в виде мицелий. На яровой пшенице она проявляется в период стеблевания, но из-за высокой температуры (27-30°С и более) и низкой относительной влажности воздуха или прохладной и дождливой погоды в июле-августе дальнейшее развитие болезни не происходит. На опытном поле НПЦ им. А.И. Бараева (Акмолинская область) из 7 видов многолетних злаковых трав, мучнистой росой поражался только пырей бескорневищный. На костре безостом, двух видах житняка и волоснеце ситниковом заболевание не обнаружено. В Восточно-Казахстанской области весной – в начале стеблевания наблюдали сильное поражение (до 50-75%) озимой ржи мучнистой росой, что указывает на перезимовку патогена на всходах в виде мицелий. Однако заболевание не переходило на яровую пшеницу, что свидетельствует о паразитировании на ней специализированной формы гриба (Койшыбаев, 1999).
В Западной Сибири возбудитель мучнистой росы перезимовывает в сумчатой стадии на послеуборочных остатках пшеницы. Аскоспоры созревают весной и заражают яровую пшеницу. В течение вегетации растений гриб развивается в конидиальной стадии, споры разносятся воздушными потоками, распространяя болезнь. Оптимальная температура для их прорастания в пределах 15-20°С, относительная влажность воздуха – 96-99%, минимальная – 4-5 и 50-70%. Массовое созревание аскоспор и интенсивное их выбрасывание из клейстотециев наблюдаются при температуре 12-17°С. Сильное развитие болезни происходит при относительной влажности воздуха в летний период 70-80% и температуре 18-19°С, чередовании влажной и сухой погоды, когда днем у растений падает тургор (Гешеле, 1956).
Распространение и вредоносность. Многолетние наблюдения показали, что на озимой и яровой пшенице мучнистая роса распространена в лесостепной зоне северного, в горно-степной и степной зонах восточного, заметно развивается на поливных землях юго-восточного и южного регионов Казахстана. В 1999 году, который отличался влажным и теплым летом, она заметно развивалась в Костанайской области, пораженность листьев яровой пшеницы достигала 25-50%. Она также широко распространена на орошаемых посевах пшеницы республик Центральной Азии, интенсивно развивалась в Иссык-кульской, Таласской, Чуйской долинах Кыргызстана (Койшыбаев, 1999). Как указывают Л.П. Сочалова и И.Е. Лихненко (2011), в лесостепной зоне Западной Сибири происходят спорадические вспышки болезни на яровой пшенице. В Краснодарском крае наблюдается стабильно высокая поражаемость ею озимой пшеницы (Роженцова, Шуляковская, 2005). В Нижнем Поволжье мучнистая роса распространена в основном на орошаемых посевах, на всходах яровой пшеницы развивается конидиальная стадия гриба, аскоспоры, формирующиеся на пораженных листьях, осенью заражают всходы озимой пшеницы. При повышенных температурах и пониженной относительной влажности воздуха заметно снижается репродуктивная способность гриба. К восковой спелости клейстотеции со зрелыми аскоспорами составляют на озимой пшенице 48%, яровой – 38% (Нечипоренко, 1988).
При поражении мучнистой росой снижаются ассимиляционная поверхность листьев пшеницы и масса зерна, уменьшается сумма углеводов, что связано с усилением дыхания растений и замедлением интенсивности фотосинтеза, активности фермента протеазы, увеличивается сумма азотистых веществ (Васягина с соавт., 1968).
Септориозные пятнистости
Основные возбудители болезней – Stagonospora (Septoria) nodorum Berk., Septoria tritici (Rob. et Desm.)
Симптомы болезни, видовой состав, морфологические и биологические особенности возбудителей. В Казахстане на пшенице зарегистрировано 5 видов грибов рода Septoria: S. tritici Rob. et Desm., S. nodorum Berk., S. gramineum Desm., S. didickeana Bayd. et Picb., S. triticiana.
В 1960 году S. nodorum обнаружен в Акмолинской области на мягкой пшенице. Основной его ареал находится в Западной и Восточной Сибири, Алтайском и Приморском краях России, а также в Прибалтике. Кроме пшеницы, он поражает ячмень и дикорастущие злаки, в частности Poa pratensis, Aegilops cylindrica (Бызова с соавт., 1971).
Более поздние исследования показали, что из видов рода Septoria, описанных в качестве патогенов пшеницы, доминирующими являются S. nodorum и S. tritici. Первый вид широко распространен на Южном Урале, в северо-восточном и северном регионах Казахстана, встречается реже в Западной Сибири, Южном Казахстане и Кыргызстане (Васецкая, Борзионова, 1987). В Северо-Западном регионе и Центральной Черноземной зоне России распространены на пшенице 3 вида возбудителя септориоза: Septoria tritici, Stagonospora nodorum и S. avenea f. sp. tritici. Во всех агроклиматических зонах доминирует первый вид, встречаемость его в среднем составляет 61-65%, второго вида 20-25% (Гультяева с соавт., 2005, Судникова, с соавт., 2005).
Характер проявления болезни зависит от видового состава возбудителя и пораженногооргана. Гриб S. tritici поражает в основномлистья и их влагалище, где заболевание проявляется в виде продолговатых желтовато-коричневых полос или темно-бурых пятен с пепельно-серым центром, которые постепенно разрастаются, и, сливаясь, образуют большие некротические полосы, листья преждевременно засыхают [рис. 9а и б]. Впоследствии на обеих сторонах листьев образуются черные точки – пикниды шаровидные или шаровидно-эллипсоидальной формы, располагающиеся беспорядочно, диаметром 75-270 мкм, овальным или круглым отверстием или устьицем. В каждой пикниде могут образовываться до 15-20 тыс. пикноспор; они по форме прямые или слегка согнутые, нитевидные, зеленоватые или почти бесцветные, с закругленными концами, 3-4, реже 5-7 перегородками, размером 36-98 × 3,5-5 мкм (Васецкая, Борзионова,1987).
Рисунок 9. Листья и колосья пшеницы, пораженные септориозом (а, б), возбудители S. tritici и S. nodorum (в и г)
S. nodorum поражает все органы растений: листья и их влагалище, междоузлия стеблей, колосковые пленки и зерно пшеницы. На листьях, часто на верхней части и по краям развиваются бурые расплывчатые пятна, которые, сливаясь между собой, приводят к преждевременному их отмиранию. Часто наблюдаются нетипичные формы болезни в виде хлоротичных пятен и некроза листьев, особенно на повторных посевах пшеницы, что возможно связано с расовым составом патогена. Поражаются болезнью и междоузлия стеблей, где образуются белесоватые или бурые расплывчатые пятна, заметные в период налива зерна. В отдельные, наиболее увлажненные годы, симптомы болезни проявляются на колосковых пленках в виде овальных бурых пятен с фиолетовым окаймлением [рис. 9a и б], особенно у подгона, и происходит заражение семян. В условиях Казахстана с засушливым климатом пикнидиальное спороношение гриба на пораженных органах пшеницы формируется в основном в осенне-весенний период. Пикниды располагаются глубоко под эпидермисом, темно-коричневые, шаровидные, 40-250 мкм в диаметре, или овальные с округлым устьицем. Пикноспоры прямые или слегка изогнутые с 1-3 перегородками, размером 18-33 × 2-4 мкм [рис. 9в и г]. Известна сумчатая стадия возбудителей септориоза Leptosphaeria nodorum Mull. и L. tritici Mull, которая развивается в неблагоприятных для патогена условиях, значительно повышая потенциал инокулюма (Бызова с соавт., 1971).
В сухо-степной и засушливо-степной зонах Акмолинской области доминирующими на пшенице являются: S. nodorum, встречаемость его варьировала от 70 до 100%, S. tritici – 12,5%, S. avenea – до 5% (Бабкенова, 2016). При поражении пшеницы грибом S. avenae на листьях, чаще вдоль главной жилки, образуются удлиненные узкие пятна с черными точками – пикнидами, которые располагаются параллельными рядами. Это заболевание менее вредоносно по сравнению с септориозами, вызываемыми S. nodorum и S. tritici.
Пикноспоры возбудителей септориоза распространяются, в основном, с каплями дождя, при наличии капельно-жидкой влаги они начинают прорастать при широком диапазоне температуры –от 5 до 35°С; оптимальная для S. nodorum – 15-20°C. Специальные опыты с имитированием дождя показали, что в каплях размером 600 мкм обнаруживается более 100 спор этого гриба (Пыжикова, Санина, 1987). На пожнивных остатках растений жизнеспособность их сохраняется до 6-18 месяцев, в верхнем слое почвы – 30-50 суток. Под воздействием сапрофитной микрофлоры и избыточной влаги они через 2-3 недели теряют всхожесть в пахотном горизонте почвы (Васецкая, Чигирев,1987).
Заражение пшеницы грибами S. nodorum и S. tritici возможно при температуре от 5 до 35°С, оптимальная – 20-30°С. Для первого патогена достаточно наличие капельно-жидкой влаги в течение 4-5 ч, для второго – 8-10 ч. При постоянной росе или капельках дождя успешное заражение листьев происходит при температуре 10-15°С за 36-48 ч., при 20-25°С – через 24-36 ч. При чередовании влажного периода с сухим, часто наблюдаемое в природных условиях, возможно заражение растений, но заболевание проявляется слабее. На сухих листьях пшеницы споры возбудителей септориоза сохраняли жизнеспособность в течение 8-10 ч. и при благоприятных условиях заражали растения (Пыжикова, Санина,1987).
В Северном Казахстане сильное развитие септориоза на яровой пшенице наблюдается в годы с повышенным количеством осадков в июне – августе, при высокой влажности воздуха (70% и более) и гидротермическом коэффициенте 1-1,5 и более (Койшыбаев, 1999; 2010).
Специализация и источники инфекции. S. nodorum широко специализирован, кроме пшеницы, поражаются райграс высокий, кострец безостый, регнерия северокавказская, овсяница луговая, эгилопс цилиндрический, пырей гребенчатый, ломкоколосник сибирский, рожь и ячмень. На листьях инокулированных растений некрозные пятна образуются через 12-15 суток, пикниды – 14-35. При заражении пшеницы реизолятами S. nodorum из злаковых трав на её листьях развивались характерные симптомы болезни, что свидетельствует о широкой специализации патогена. Кроме диких злаков, гриб поражает эспарцет, одуванчик и гречиху с образованием на пятнах пикни; люцерна, клевер и марь белая не поражались (Васецкая, Борзионова, 1986).
Наши многолетние наблюдения не подтвердили широкую специализацию S. nodorum и S. tritici. В Северном Казахстане в годы эпифитотийного развития септориоза на яровой пшенице, не поражались им овес, ячмень и озимая рожь. При искусственной инокуляции злаков грибом S. nodorum, характерные признаки болезни проявлялись только на озимой и яровой пшенице, хлорозные пятна и некрозы – на мышее сизом, костре безостом, не поражались сорго, кукуруза, суданская трава, просо, овес и ячмень (Койшыбаев, Исмаилова,1991).
Источниками инфекции септориоза могут быть семена, а также пожнивные остатки растений из семейства злаковых. Однако роль их неодинакова для разных почвенно-климатических зон. В Западной Сибири одним из источников инфекции являются семена пшеницы, заболевание проявляется в период всходов на колеоптиле и листьях (Чулкина с соавт., 1987).
Анализы образцов семян пшеницы, полученных из различных регионов Казахстана, путем проращивания на бумажных рулонах в лаборатории и в чашках Петри под ультрафиолетовыми лучами в специальных боксах при температуре 15-20°С показали, что пораженность всходов септориозом не превышает 1-3%. На посевах пшеницы с высоким травостоем (70-80 см и более), колосковые пленки не поражаются септориозом, или заболевание проявляется в слабой степени (до 5-10%), очень редко наблюдается формирование на них пикнид. При проращивании образцов семян, отобранных из пораженных септориозом колосьев, количество всходов с характерными признаками болезни не превышало 5-10%. Проявление болезни в северном регионе в период стеблевания-колошения яровой пшеницы также свидетельствует о второстепенной роли семян в передаче инфекции. В юго-восточном регионе на озимой пшенице признаки септориоза проявляются рано – в период стеблевания растений, что связано с благоприятными условиями погоды в конце весны и начале лета: в мае- июне часто выпадает до 100-150 мм осадков (Койшыбаев, 2001, 2010).
Многолетние исследования показали, что в северном и других регионах Казахстана, инфекция септориоза сохраняется на пожнивных растительных остатках пшеницы. Пикниды и споры S. nodorum формируются обычно в осенне-весенний период, а в наиболее увлажненные годы летом – на листьях и колосковых пленках. На пожнивных её остатках пикноспоры дозревают не одновременно, на отрезке соломы можно обнаружить вполне зрелые пикниды, с которых высвобождаются споры, находящиеся в начальной стадии формирования. На площади листьев 1 см2 и междоузлиях стебля образуются до 300-400 пикнид S. tritici, что свидетельствует о высоком инфекционном потенциале возбудителя.
Лабораторные опыты показали, что споры S. nodorum прорастают очень быстро и при низкой температуре, так, при 12-15°С через 1-2 часа всхожесть их составляла 20-27%, через 3 часа – 64%. Споры S. tritici прорастали очень медленно: при температуре 15°С через 12 часов количество проросших спор составляло 6,3%, 20°С – 13,2%, в то же время у первого вида 90-100%.
Распространение и вредоносность. Септориоз – широко распространенная и очень вредоносная болезнь пшеницы в США и Канаде, Западной Европе и во многих странах мира. Заболевание, нызываемое Stagonospora nodorum, чаще встречается в Северной Европе, восточной части США, на западе Австралии, Septoria tritici превалирует в регионах с умеренным климатом (Schauen, 1999). Если в 1980-90 гг. в Российской Федерации септориоз имел локальное распространение, то в последние годы встречается повсеместно. В Центрально – Черноземной зоне и Западно-Сибирском регионе в структуре патогенных комплексов доля возбудителей этой болезни достигает 45-55%, в 2007 г. при эпифитотийном её развитии, потери урожая составили 20-25%. В Краснодарском крае также участились массовые вспышки болезней, вызываемые грибами из рода Septoria, значительно снижающие продолжительность функционирования листового аппарата пшеницы. В более засушливом Поволжском агроклиматическом регионе пораженность посевов пшеницы септориозом во влажные годы достигает 30-40%, доминирующим видом является Septoria tritici. В 2003-2005 гг. на Северо-Западном регионе он основной возбудитель септориоза, что связано с потеплением климата (Судникова с соавт., 2005; Гультяева с соавт., 2005; Назарова с соавт, 2010).
В Белоруссии септориоз и желтая пятнистость, фузариоз колоса и корневые гнили являются основными болезнями озимых зерновых культур, потери от их комплекса могут достигать 30-35% (Буга с соавт., 2012).
В Северном Казахстане заметное развитие септориоза на яровой пшенице зарегистрировано в конце 70-годов прошлого столетия. В 1986 г. он развивался до уровня эпифитотии, охватывая до 50,4-62,9% площадей её посевов, на 1/3 части проявлялся в средней и сильной степени. В 1993-1994 гг. на площади 1,5-2,3 млн. га заболевание было распространено сильно, вызывая заметные потери урожая зерна, а в засушливые 1995-1998 гг. – в слабой степени. Септориоз, вызываемый S. nodorum, развивается заметно почти ежегодно, за исключением острозасушливых, S. tritici, – в основном в годы с обильными осадками и низкой температурой воздуха в период стеблевания-колошения пшеницы.
В южном и юго-восточном регионах Казахстана и Кыргызской Республике септориоз является наиболее распространенной болезнью озимой пшеницы. В годы с влажной (сумма осадков в апреле и мае не менее 75-100 мм) и прохладной весной (15-20°С) развивается до уровня эпифитотии. На одном и том же листе одновременно встречаются септориоз и желтая пятнистость (Койшыбаев, 2010).
В результате преждевременного отмирания ассимиляционной поверхности листьев, междоузлий стебля и колосковых пленок пшеницы, значительно снижается фотосинтеническая активность растений, сокращается их вегетационный период. Потери урожая зерна происходят в основном в результате снижения озерненности колоса и массы зерна у больных растений. Установлено, что вредоносность септориоза зависит от степени пораженности листьев: при 30% урожай снижается в среднем на 10%, 30-50 – 20%, при 51-75 – на 30% и свыше 75% – на 40%. Отмечено, что между степенью поражения колоса озимой пшеницы септориозом и содержанием в зерне клейковины существует отрицательная корреляционная связь (r= −0,69), при увеличении пораженности его на 10% она снижается на 2,5% (Пыжикова, Санина 1987; Санин, Жохова, 2012).
В юго-восточном Казахстане при слабом развитии септориоза масса 1 000 зерен озимой пшеницы снижалась на 1,9-4,6%, умеренном – 10-12%, сильном – до 19,3-27,9%. Установлена высокая коррелятивная зависимость между пораженностью листьев и снижением массы 1 000 зерен (r= −0,96). Наибольшие потери отмечаются при развитии патогенов на колосковых пленках, между поражением колоса и потерями урожая существует тесная коррелятивная связь (Койшыбаев, Исмаилова, 1999).
В 1986 г. при эпифитотийном развитии болезни в Северо-Казахстанской области у сорта Омская 18 в контрольном варианте масса 1000 зерен не превышала 22 г, при обработке посевов Тилтом составляла 31,2-34,6 г. В 1992 г. при умеренном развитии бурой ржавчины и септориоза (25-50%) в Костанайской области, урожай сортов яровой пшеницы Иртышанка 10 и Целинная-Юбилейная снизился на 13,3%, в 1993 г. – при сильном их развитии потери составляли 33,7-38,1%; в контроле масса 1 000 зерен была ниже на 19,3 и 29%, т.е. формировалось щуплое зерно [табл. 6].
Таким образом при раннем проявлении и эпифитотийном развитии септориоза совместно с листовой ржавчиной в результате снижение озерненности колоса и массы зерна потери урожая могут достигать 25-30% и более, при позднем проявлении и умеренном развитии 7-10%.
Гельминтоспориозные пятнистости листьев
Пшеница поражается двумя видами гельминтоспориозных пятнистостей: темно-бурой (возбудитель – Bipolaris sorokiniana Sacc., син: Helminthosporium sativum P. K. et B.) и желтой – Drechlera tritici – repentis (Died.) Shoem. ; сумчатая стадия – Phyrenophora tritici-repentis. Они широко распространены во многих странах, обычно встречаются одновременно с преобладанием того или иного вида в зависимости от
агроклиматических зон и погодных условий (Duveiller, Dubin, 2003).
Темно-бурая пятнистость. Проявляется на листьях пшеницы в виде округлых светло-бурых пятен, которые при высокой влажности воздуха покрываются темно-оливковым налетом, состоящим из конидий и конидиеносцев гриба. Возбудитель болезни поражает и подземные органы растений, вызывая корневую гниль, развивается также на зародышевой части зерна. Полные сведения о биологических и морфологических особенностях возбудителя приводятся в подразделе корневая гниль.
Желтая пятнистость листьев (пиренофороз)
Симптомы, морфология возбудителя и распространение болезни. Симптомы очень сходны с признаками септориоза, вызываемого грибами Septoria nodorum и S. tritici. Поражаются листья, на которых сначала появляются округлые, эллипсоидальные, желтые, светло-коричневые пятна, с хлоротичной зоной вокруг, которые быстро увеличиваются в размере, часто сливаются между собой, образуя широкие полосы [рис. 10а и б]. Заболевание проявляется на междоузлиях стебля в виде темно-бурых или светлых расплывчатых пятен, реже на колосковых пленках. Максимальное развитие болезни происходит в период колошения – молочной спелости зерна, при сильном поражении начиная с верхушки листья засыхают. На пораженных органах растений при высокой влажности воздуха развиваются мицелий и спороношение гриба серовато-белого или темно-серого цвета. Конидиеносцы выходят из устьиц листьев группами или одиночно, длина их от 10-20 до 400 мкм, конидии – прямые или слегка изогнутые, цилиндрические, желтоватые или желтовато-коричневые, размером 20-75-270 × 10-24 мкм, количество перегородок от 2-3 до 8-10. Гриб имеет сумчатую стадию – Pyrenophora tritici repentis Drechs. [рис. 10в], которая формируется на пожнивных остатках растений.
Рисунок 10. Листья пшеницы пораженные желтой пятнистостью (а); конидиальная (б) и сумчатая стадия (в) возбудителя болезни
Установлено, что в условиях Узбекистана возбудитель болезни перезимовывает на листьях пшеницы в виде покоящихся мицелий, а также на послеуборочных её остатках и дикорастущих злаках в сапрофитной стадии. Источником инфекции могут быть и семена. Заражение растений возможно при температуре 5°С и продолжительности росяного периода 2 ч. Оптимальная температура для роста и спороношения гриба D. tritici-repentis – 20-25°С, частые и обильные осадки усиливают развитие болезни. Гриб, кроме пшеницы, поражает разные виды пырея (Agropyron repens, A. interruptum), житняк (A. cristatum), щетинник (Setаria viridis), эгилопс (Aegilopus cylindrica), костер безостый (Bromus inermis), ячмень дикий (Hordeum spontaneum), суданскую траву (Sorghum sudanense). В опытах Л. Ламари с соавторами при искусственной инокуляции грибом 16 видов злаков, характерные симптомы болезни обнаружены только на пшенице и тритикале (Постникова, 1999; Postnikova, Khasanov, 1999). В 2004 г. в предгорной зоне Алматинской области на озимой ржи, растущей от самосева в посевах озимой пшеницы, обнаружены типичные симптомы желтой пятнистости (Койшыбаев, 2010).
Для прорастания конидии видов Helminthosporium, Drechslera наиболее благоприятна температура от 18 до 32°С и высокая влажность воздуха. На поверхности листьев конидии прорастают в течение 4-х ч., мицелий внедряется в ткань растений через 8 ч., в течение суток интенсивно распространяется на соседние клетки растения-хозяина (Dubeiller, Dubin, 2013). Специальные опыты показали, что образование конидиеносцев происходит при свете, т.е. днем, конидии – в темноте при высокой влажности воздуха или наличии капельно-жидкой влаги; при сухой погоде они рассеиваются и повторно заражают растения (Fsans, 1998).
Желтая пятнистость или пиренофороз сравнительно новое заболевание пшеницы, она широко распространена во многих странах мира. В начале 40-годов прошлого столетия впервые обнаружена в США и Канаде, в 80-90 годы – в странах Западной Европы. В восточной части Канады желтая пятнистость и септориоз встречаются в комплексе; первое заболевание в более засушливой зоне, второе – в наиболее увлажненной. Совместно с гельминтоспориозным ожогом она является широко распространенной болезнью пшеницы в странах Южной Азии, где возделывают её в рисово-пшеничных севооборотах. Усилению её вредоносности способствуют возделывание восприимчивых сортов и широкое внедрение нулевой технологии возделывания.
Во многих регионах потери урожая от комплекса гельминтоспориозных болезней варьируют от 15 до 27%, в Мексике на отдельных, не коммерческих сортах – от 50 до 90%. В последние годы желтая пятнистость стала широко распространенной болезнью пшеницы в Австралии и совместно с септориозом обусловливает потери урожая от 5 до 20% (Saary,1998; Baconyi, Aponyi, Fischl 1998; Fernandes,
DePauw et all., 1998; Ozoria et all., 1998; Dubeiller, Dubin, 2013).
В России и других странах СНГ проблема желтой пятнистости возникла в 80-годы прошлого столетия. Впервые она была обнаружена в 1985 году в Северном Кавказе, в настоящее время стала широко распространенной болезнью этой культуры в северо-западном регионе Поволжья, Западной Сибири и Алтайском крае. В 1986-1988 гг. происходило эпифитотийное её развитие в Краснодарском и Ставропольском краях Российской Федерации. Выявлена высокая зависимость степени поражения посевов болезнью от влагообеспеченности зоны: в регионах с достаточным увлажнением показатель достигал 40-60%, а в засушливых – 5-10% (Михайлова и др., 2005; Кремнева, 2012; Волкова с соавт., 2012; Левитин, 2012).
В Центральной Азии желтая пятнистость была обнаружена в середине 80-х годов в Узбекистане на озимой пшенице, наибольшее её развитие (70-80%) происходило в Джизакской области на высоте 700-900 метров над уровнем моря и выше (Хасанов,1988). Мониторинг болезней пшеницы в период 2003-2009 гг. в разных агроклиматических зонах Таджикистана показал, что она стала доминирующей этой культуры. Если в 2004-2005 гг. её соотношение с желтой ржавчиной было примерно одинаковое – около 40-50%, то в 2006-2009 гг. достигло 90-100% (Rahmatov et all, 2009).
Желтая пятнистость широко распространена на озимой и яровой пшенице в южном, юго-восточном и северном регионах Казахстана. В 1996 и 2001 гг. происходило эпифитотийное ее развитие в предгорной зоне Алматинской области. Первые признаки заболевания были обнаружены в период стеблевания озимой пшеницы, в фазу колошения пораженность листьев верхнего яруса составляла 25-50%, к молочной спелости зерна достигала 75-100%, и они засыхали преждевременно. В северном регионе республики заметное развитие желтой пятнистости на яровой пшенице происходило в 1999, 2000, 2007 гг., особенно по стерневому фону. Широкое её распространение и усиление интенсивности её развития связано с монокультурой пшеницы или чрезмерной насыщенностью ею севооборотов, минимальной обработкой почвы, сохранением стерни, самое главное, высокой восприимчивостью к патогену возделываемых сортов. В предгорной зоне юго-восточного региона многие сорта, в том числе, Стекловидная 24, Жетысу и другие, поразились желтой пятнистостью до 50-75% (Хасанов, 1988; Койшыбаев, 1999).
Л. Ламари (Lamari, 2005) на основе мониторинга посевов пшеницы в странах, расположенных по шелковому пути, относит Казахстан к региону широкого распространения и высокой вредоносности желтой пятнистости, Кыргызстан и Азербайджан – среднего, Узбекистан – слабого проявления. В 2003 г. совместно с представителем СИММИТ Е. Дювейллером и профессором Католического Университета Бельгии Г. Марайте проводили фитосанитарный мониторинг посевов пшеницы в центральном и северном регионах Казахстана и Западной Сибири. Обращалось внимание на стерневые остатки, на многих полях находили сумчатую стадию гриба Ph. trititci repentis. Для идентификации видового состава возбудителей болезней были собраны стерневые остатки из более 50 полей пшеницы, которые анализированы в лаборатории департамента фитопатологии указанного университета под руководством профессора Г. Марайте. Установлено, что из пораженных её органов частота выделения гриба D. tritici-repentis варьирует от 12 до 31%, в среднем составляет 21%, S. nodorum – не превышал 15%, что, на наш взгляд, связано с формированием пикнид и пикноспор на пожнивных остатках осенью или весной следующего года. Об этом косвенно свидетельствует отсутствие спороношения грибов на 44% анализированных сегментах. Кроме того, из септориальных пятен часто выделялся Alternaria
alternata, который заселяет ткани растений, некротизированными грибами и бактериями [табл. 7].
Для уточнения частоты встречаемости грибов D. tritici-repentis, а также Septoria nodorum и S. tritici были анализированы гербарные материалы озимой пшеницы, собранные в 2003 г. во время мониторинга посевов в южном и юго-восточном регионах Казахстана и Кыргызской Республике. Установлено, что D. tritici-repentis выделяется от 4,8 до 16,8%, S. nodorum и S. tritici – от 5 до 13,3%, Bipolaris sorokiniana –
17,1-20% [табл. 8]. Более высокая встречаемость последнего, вероятно, обусловлена погодными условиями года: в Алматинской области выпало осадков в 2-3 раза больше многолетней нормы. В результате высокой влажности воздуха происходило заражение листьев нижнего и среднего ярусов этой культуры темно-бурой пятнистостью.
Таблица 7. Частота выделения дематиевых грибов из листьев яровой пшеницы в Казахстане и Западной Сибири
Таблица 8. Частота выделения несовершенных грибов из листьев озимой пшеницы в южном Казахстане и Кыргызстане
В 2006-2007 гг. в степной зоне Акмолинской и Костанайской областей на стерневых остатках повторных посевов пшеницы весной находили зрелые псевдотеции D. tritici repentis (на отрезке 5-10 см до 15-20 штук), что свидетельствует об огромном запасе инфекции патогена.
Корневые гнили
Пшеница поражается несколькими видами корневых гнилей, различающихся по внешним признакам проявления болезней и видовому составу возбудителей. В степной зоне Северного Казахстана на яровой пшенице преобладает гельминтоспориозная или гельминтоспориозно-фузариозная гнили. В горной зоне юга и юго-востока на озимой пшенице, наряду с гельминтоспориозной, распространены офиоболезная корневая гниль и снежная плесень. В Западном Казахстане в условиях орошения на её посевах обнаружен церкоспореллез, или ломкость стеблей (Койшыбаев, 2002).
Гельминтоспориозная (обыкновенная), гельминтоспориозно-фузариозная гнили
Возбудители болезни – Bipolaris sorokiniana Sacc. (Helminthosporium sativum P. K. et B.) и виды рода Fusarium Link.
Симптомы болезней, видовой состав, морфологические и биологические особенности возбудителей. Проявляется на первичных и вторичных корешках, эпикотиле, подземных междоузлиях, у основания стебля пшеницы в виде темно-бурых, коричневых штрихов, пятен или широких полос [рис. 11а]. При сильном развитии болезни происходит сплошное побурение одного или двух междоузлий, отмирание боковых стеблей. Пораженные органы растений во влажной камере покрываются темно-оливковым, бархатистым налетом, состоящим из мицелий, конидиеносцев и конидий гриба. Конидиеносцы – коленчато-изогнутые, зубчатые, с 5-8 перегородками, конидии – оливковые, темно-оливковые, прямые, реже изогнутые, булавовидные, обратно-яйцевидные, с 2-7 перегородками [рис. 11б].
Гриб H. sativum широко специализирован, поражает более 90 видов злаков, в т.ч., пшеницу, ячмень, рожь, овес, разные виды пырея, мятлика, овсяницу и др. ; некоторые исследователи выделяли его из двудольных растений (вьюнок полевой, осот розовый, полынь горькая, марь белая и др.). Однако в природных условиях круг растений, поражаемых патогеном, ограничен. Наши исследования показали, что овес, овсюг, рожь, просо, могар, кукуруза, житняк и др. практически устойчивы к этой болезни. При наличии капельно-жидкой влаги гриб развивается при температуре от 3-5 до 35-40°С, оптимальная – 20-27°С. Лабораторные опыты с чистой его культурой показали, что наиболее оптимальная температура для его развития находится в пределах 20-30°С [рис. 12].
Рисунок 11. Гельминтоспориозная (обыкновенная), гельминтоспориозно-фузариозная гнили (а) и ее возбудитель (б)
В странах с теплым и влажным климатом, в частности, в Южной Америке и Юго-Восточной Азии гриб Bipolaris sorokiniana является возбудителем гельминтоспориозного ожога листьев пшеницы. В последние годы он заметно прогрессирует, что связано с широким внедрением пшенично-рисовых севооборотов, где создаются благоприятные условия для накопления инфекции (Saari,1998; Ginkel, Rajaram, 1998).
Возбудителями корневых гнилей озимой и яровой пшеницы также могут быть грибы из рода Fusarium, в частности F. avenaceum Sacc., F. gibbosum App. et Wr., F. graminearum Schw., F. oxysporium Snyd. et Xans.
При фузариозной корневой гнили больные корешки и подземные междоузлия стебля покрываются ватообразным белым, желтоватым или розовым спороношением гриба. Макроконидии серповидной формы с 2-3 до 5-7 перегородками, микроконидии одноклеточные, яйцевидные или грушевидные.
Установлено, что видовой состав возбудителей может варьировать в зависимости от зоны возделывания пшеницы. В горных и предгорных районах южного и юго-восточного региона, где в основном возделывают озимую пшеницу, доминирует F. graminearum, а в степной зоне северного и западного регионов на яровой пшенице – F. oxysporium и F. аvenaceum (Ермекова, Рысбаева, 1978). В Восточной Сибири из пораженных органов яровой пшеницы гриб B. sorokiniana выделялся с частотой до 74,9-81,5%, виды Fusarium – не более 6,5-9,9% (Хацкевич, Бенкен, 1987).
Рисунок 12. Влияние температуры на рост гриба Bipolaris sorokiniana в условиях in vitro: слева при температуре 25°С, в середине – 20, справа – 10-12°С
На поливных землях Узбекистана возбудителями корневой гнили озимой пшеницы являются Fusarium culmorum, F. gibbosum, F. momiliforme, а также H. sativum, Рythium de Barianum и Rhizoctonia solani. При посеве пшеницы по пару доминировали виды Fusarium, по стерне – H. sativum Наибольшей вирулентностью обладает F. culmorum, который значительно снижает всхожесть семян (Гольд-штейн и др., 1972).
Источники инфекции. Возбудители корневых гнилей в основном сохраняются на пораженных растительных остатках и в почве, иногда передаются семенами. При отсутствии восприимчивого растения-хозяина, гриб может сохраняться в почве в виде диаспор. В Северном Казахстане основными источниками инфекции являются послеуборочные остатки пшеницы и дикорастущих злаков, конидии Helminthosporium из них выделялись от 20 до 69%, виды Fusarium от 3,3 до 23,3% соответственно (Джиембаев, Альжанов, 1970).
В Джизакской, Кашкадарьинской, Сухандарьинской областях Узбекистана, в Чарджоуской и Кулябской Таджикистана, в Таласской области Кыргызстана, а так же в западном, южном, юго-восточном, северном, восточном регионах Казахстана конидии B. sorokiniana обнаружены в приземном слое воздуха на высоте 50-500 м (Хасанов, 1987).
В Западной Сибири основными источниками инфекции корневой гнили пшеницы являются культурные и дикорастущие злаки –ячмень, щетинник и овсюг. Возбудитель болезни успешно выживает в почве, зараженность её патогеном с севера на юг увеличивается в 3-4 раза. Установлено, что в условиях Восточной Сибири в воздушно-сухой почве при температуре 18-23°С конидии сохраняют жизнеспособность в течения 131 суток, а при постепенном ее увлажнении всхожесть их снижается до 50-60%. Пороговый уровень инфицированности им составляет 15-20 конидий B. sorokiniana на 1 г почвы, что близко к плотности популяции гриба в целинных и залежных землях, зависит от типа почвы: 10%-ое развитие болезни, когда достоверно снижается урожай, на обыкновенных черноземах наблюдается при её инфицированности 50 конидий. Более слабое проявление болезни наблюдается при плотности почвы 1,0-1,2 кг/см3, при низком –0,9 кг/см3 и высоком индексах усиливается её развитие. Оно также зависит от влажности почвы, при 40-60% от полной влагоемкости к концу вегетации пшеницы индексы болезни не превышают 11-14%, а при варьировании от 25 до 60% увеличиваются до 65%. При температуре до -30-40°С патоген сохраняется в почве до 7 месяцев (Чулкина с соавт., 1975; Бенкен, Хацкевич,1987; Чулкина, Павлова, 1987).
Корневая гниль также передается семенами пшеницы, при этом всходы поражаются болезнью до 14-56%, происходит снижение их всхожести (Шевченко,1970). Фитоэкспертиза семян пшеницы урожая 1986-1988 гг. из различных регионов Казахстана показала, что количество семян с признаками «черного зародыша» варьирует от 3-5 до 30-40%. Корреляционный анализ показал, что имеется определенная связь между пораженностью всходов корневой гнилью и инфицированностю семян (r=0,46), которая свидетельствует об их роли в передаче инфекции болезни (Койшыбаев, 1981).
Распространение и вредоносность. С.М. Тупеневич (1970) еще в 40-х годах прошлого века указывал, что гельминтоспориоз является наиболее широко распространенной болезнью зерновых культур в южных областях Советского Союза. Неустойчивый водный режим в этом регионе способствует усилению восприимчивости растений к заболеванию. Корневая гниль распространена очень широко и является наиболее вредоносной болезнью яровой пшеницы в Казахстане и азиатской части Российской Федерации. Исследования в Акмолинской области в начале 60-х годов на базе Всесоюзного института зернового хозяйства показали, что корневые гнили на яровой пшенице в первые годы распашки целинных земель развивались незначительно (Краева, 1960; Джиембаев, 1971). Постепенно шло накопление инфекции в почве и усиливалось развитие болезни. В 1966 г. на Кокшетауской опытной станции распространение болезни на коммерческих сортах пшеницы варьировало от 24,2 до 40,5%, при слабом ее проявлении урожай снижался на 11,6%, сильном – до 42,5% (Городилова, Шевцов,1972).
В результате поражения корневой системы растений нарушается коммуникация между надземными и подземными органами, что ухудшает снабжение их элементами минерального питания и водой. Влияние болезни на рост растений наблюдается в фазу всходов, снижается всхожесть семян пшеницы, сила их роста, в дальнейшем больные растения заметно отстают от здоровых (Чулкина, 1975). Исследования показали, что корневая гниль влияет на физиолого-биохимические процессы и качество зерна. В 1 г абсолютно сухого вещества у здоровых растений содержание общего азота составляло 3,1%, белка – 15,3, растворимых углеводов – 5,1, крахмала – 48,9%, у больных –2,84; 13,8; 4,7 и 40,1% соответственно (Джиембаев, 1971).
Вредоносность корневой гнили заметно варьирует в зависимости от сорта пшеницы, поражаемого органа, степени развития болезни, предшественников и погодных условий. В Западной Сибири при эпифитотии корневых гнилей, наблюдавшихся в 50-60 годы прошлого века, потери её урожая составляли от 14-15 до 45-50%, ухудшалось качество зерна и семян (Шевченко,1970; Чулкина, Павлова,1987).
В засушливо-степной зоне Павлодарской области при поражении корневой гнилью нижнего междоузлия стебля потери урожая яровой пшеницы составляли 12,5%, основании стебля – 15,2%, обоих органов – 61,5- 69,1%. При посеве пшеницы по пару, потери урожая не превышали 2,1-4,4%, одноименному предшественнику второй год – 5,8-9,3%, после кукурузы – 2,2-5,6% (Бедина, 1974). На Карабалыкской опытной станции у сорта твердой пшеницы Безенчукская 98 в условиях достаточного увлажнения (ГТК 1,18) урожай от болезни снижался на 19%, в засушливые годы (ГТК 0,65) – на 44,2% (Тупеневич, Нестеров,1977).
Вредоносность корневой гнили резко возрастала при повреждении растений скрытостеблевыми вредителями. Так, при слабом проявлении болезни урожай яровой пшеницы снижался на 11,6%, сильном – 42,5%, а когда растения повреждались еще вредителями, потери достигали 65,7% (Городилова,1967).
В.В. Котова (1970) в условиях Костанайской области определяла вредоносность корневой гнили яровой пшеницы. Распространение болезни в севооборотах с высоким удельным весом культуры достигало 60-100%, её развитие – 20-46%. Потери зерна в зависимости от сортов, предшественников и погодных условий года колебались от 10,7 до 30%. Ею установлено, что между интенсивностью развития болезни в фазу полной спелости зерна и продуктивностью растений существует обратная связь с коэффициентом корреляции r=−0,49-0,85. Достоверное снижение урожая начинается при развитии болезни 10-15%; порог её вредоносности выше по предшественникам пар и кукуруза, ниже при выращивании пшеницы бессменно в течение 2-3 лет. Она рекомендовала определить потери урожая от корневой гнили по уравнению:
Y = 7,84 + 0,0089X + 0,07X
Y – недобор урожая, %;
Х – интенсивность развития болезни;
Х – количество растений на 1 м2.
Наши исследования в 1976-1980 гг. в пустынно-степной, предгорной и горной зонах юго-восточного региона Казахстана показали, что корневая гниль на озимой пшенице распространена повсеместно, индекс её варьирует от 5-10 до 40-50%, более она вредоносна в пустынно-степной зоне. При средней и сильной степени поражения растений озерненность колоса снижалась от 9,6 до 33,1, масса 1 000 зерен – от 12,7 до 24,5%, при слабом – от 2,3 до 10,5%. По предшественнику пар вредоносность болезни составляла 3,5%, озимой пшенице – 5,3% [табл. 9]. В горной и предгорной зонах она проявлялась в слабой степени, и была менее вредоносной (Койшыбаев,1981; 1982).
Таблица 9. Вредоносность корневой гнили на озимой пшенице (Алматинская обл., 1976-1980 гг.)
В 1981-1985 гг. на многолетнем стационаре Торгайской СХОС определяли на яровой пшенице вредоносность корневой гнили в 5-польном зернопаровом севообороте со следующим чередованием культур: пар-пшеница-пшеница-пшеница-ячмень. Анализ структуры урожая показал, что у пораженных болезнью растений снижаются продуктивная кустистость, озерненность колоса и масса зерна, особенно при среднем и сильном её проявлении; растения заметно отстают в росте, что отражается на формировании колоса и его озерненности. Потери урожая были наименьшими при возделывании пшеницы по пару, на повторных её посевах возрастала вредоносность болезни. При слабом ее проявлении (1 балл) по предшественнику пар урожай пшеницы снижался от неё на 5%, на второй и
третьей культурах– до 9%. Вредоносность корневой гнили зависела и от погодных условий: в годы с нормальным увлажнением она была низкой, в засушливые-высокой [табл. 10].
В 1991-1993 гг. в сухостепной зоне Костанайской области определяли вредоносность корневой гнили на яровой пшенице в 4-х полном зерновом севообороте. Установлено заметное её варьирование в зависимости от погодных условий и предшественников, возрастала при возделывании этой культуры по ячменю [табл. 11].
Таблица 10. Вредоносность корневой гнили на яровой пшенице в зернопаровом севообороте (Торгайская СХОС, 1981-1985 гг.)
Таблица 11. Вредоносность корневой гнили на яровой пшенице в степной зоне Костанайской области (1991-1993 гг.)
В 1994-1995 гг. в горно-степной зоне Восточно-Казахстанской области на двух сортах яровой пшеницы определяли вредоносность корневой гнили. Анализ структуры урожая показал, что у пораженных болезнью растений сорта Кутулукской снижается кустистость, озерненность колоса и масса 1 000 зерен – на 11,6-16,6%.
В 2001-2003 гг. определяли вредоносность корневой гнили в засушливо-степной зоне Акмолинской области яровой пшеницы по двум предшественникам на трех уровнях технологии возделывания. Коэффициент вредоносности болезни был более высоким, когда её возделывали по одноименному предшественнику по обычной или упрощенной технологии, ниже по интенсивной технологии по пару. При слабом проявлении болезни, озерненность колоса и масса 1 000 зерен снижались до 5,6%, умеренном и сильном – до 13,7% [табл. 12].
Таким образом, многолетние исследования в разных почвенно-климатических зонах показали, что вредоносность корневой гнили пшеницы зависит от предшественников, условий года и технологий возделывания. В результате уменьшения кустистости, массы зерна и озерненности колоса снижается продуктивность растений. Ниже приводится коэффициент вредоносности корневой гнили на озимой и яровой пшенице в зависимости от степени ее развития
и предшественников [табл. 13].
Таблица 12. Вредоносность корневой гнили на яровой пшенице в зависимости от технологии возделывания (НПЦ ЗХ им. А.И. Бараева, 2001-2003 гг.)
Таблица 13. Коэффициент вредоносности корневой гнили пшеницы
Другие виды корневых гнилей
Церкоспореллезная или глазковая пятнистость, ломкость стеблей. Возбудитель болезни – гриб Cercosporella herpotrichoides Fron. (синонимы: Oculimacula acuformis Boer. Hamers, анаморфа – Helgardia acuformis Nirenb). Признаки болезни проявляются на нижних надземных междоузлиях озимой пшеницы, реже на влагалище листьев в виде овальных, серовато-палевых, в центре соломенножелтых, белесоватых пятен с расплывчатым краем, темно-коричневым или темно-зеленым ореолом. Характерные её признаки – глазковая пятнистость и беспорядочное полегание больных растений. Позже на пятнах образуются черные склероции, внутри стеблей – конидальное спороношение гриба: сначала белый, позже дымчато-серый мицелий, конидии – бесцветные, игольчатые, в верхней части согнутые с 5-7 перегородками. Заболевание широко распространено в странах Западной Европы, центральном и западном регионах России с прохладным и влажным климатом. Инфекция сохраняется на послеуборочных остатках растений, для развития болезни благоприятна высокая влажность почвы (Фадеев с соавт, 1986).
Офиоболезная корневая гниль. Возбудитель болезни – сумчатый гриб Gaeumannomyces graminis Sacc. Arx. et Oliv, синоним – Ophiobolius graminis Sacc. Поражаются нижние междоузлия стебля озимой пшеницы, которые полностью чернеют, в результате отмирают основные и боковые побеги. При сильном проявлении болезни наблюдается белоколосость, при умеренном – формируется легковесное и щуплое зерно. Осенью под прикрытием отмершего нижнего листа образуются шаровидные плодовые тела – псевдотеции гриба, содержащие продолговато-булавовидные, прямые или согнутые сумки с 8 аскоспорами. Они собраны в двухрядные пучки, бесцветные, серповидные с 5-7 поперечными перегородками (Фадеев с соавт, 1986).
Снежная плесень. Возбудитель болезни – Fusarium nivale (Fr.) Ges. – сумчатая стадия Calonectria graminicola (Berk et. Br.) Wr. Поражается в весенний период ослабленная при перезимовке озимая пшеница, особенно на склонах, пониженных участках с глубоким слоем снега. После его схода на перезимовавших листьях появляется паутинистый налет розоватого цвета. Часто пораженные растения погибают очагами, что приводит к изреженности посевов.
Макроконидии гриба размером 3-18 × 3-4 мкм суженные с обоих концов, в массе розовые, округленные, без ножки, с 1-3, реже 4-7 перегородками. Перитеции овальные, диаметром 1,1-0,2 мм (Фадеев с соавт., 1986). Заболевание распространено в горных и предгорных районах южного, юго-восточного и восточного регионов Казахстана, возможно в Кыргызстане и Таджикистане, имеющие аналогичные природные зоны (Койшыбаев, 2002).
Болезни зерна
На формирующемся зерне развивается эпифитная микрофлора, состоящая преимущественно из неспороносных бактерий, а также грибов Cladosporium herbicola, Alternaria tenuies и др.
Преобладание в микробном ценозе зерна бактерий Pseudomonas herbicola служит показателем его доброкачественности. В период вегетации пшеницы зерно заселяется полусапрофитными и заражается паразитными грибами, в частности из родов Helminthosporium, Fusarium, Septoria; бактериями – виды Pseudomonas, Xanthomonas и др. Кроме того, в Северном Казахстане, Западной Сибири и других регионах Российской Федерации в увлажненные в период налива зерна годы, происходит энзимно-микозное истощение семян (ЭМИС) – заболевание сложной этиологии.
При высокой влажности зерна (более 15-16%) в период хранения могут развиваться плесневые грибы, в частности виды родов Penicillium, Aspergillus, Trichotecium, Mucor и др., вызывающие снижение всхожести семян и качества товарной продукции. Развитие их возможно и при низкой температуре помещения (1-5°С), не происходит при влажности зерна 13-14% и ниже (Трисвятский,1986).
«Черный зародыш» зерна и фузариоз колоса
Возбудителиболезни – Alternariaalternata(Fr.)Keisl.,(син.: Alternaria tenuies Nees), Bipolaris sorokiniana Sacc. (син.: Helminthosporium sativum P. K. et. В.)
Симптомы, распространение и вредоносность болезни, морфологические и биологические особенности возбудителей. Заболевание развивается на зародышевой части и проявляется в виде темных пятен различной величины, особенно заметно в годы с высокой влажностью воздуха в период налива зерна. В зависимости от видового состава возбудителя различаются альтернариозный и гелминтоспориозный тип «черного зародыша». При гельминтоспориозной инфекции мицелий гриба проникает в зародыш и щиток, формируются щуплые семена с низкой лабораторной всхожестью, при их прорастании всходы поражаются корневой гнилью. Установлено, что инфицирование пшеницы грибом H. sativum происходит в период цветения – восковой спелости зерна. При альтернариозном «черном зародыше» гриб локализуется в оболочке зерна, эндосперме и алейроновом слое, всхожесть семян не снижается (Кузьмина, 1977).
Изучение этиологии «черного зародыша» пшеницы в Северном Казахстане показало, что гриб A. tenuiеs находится в плодовой оболочке, не проникает в ткань зародыша. Микологический анализ показал, что из пораженных зерен гриб H. sativum выделяется от 13,9 до 31,3%, а A. tenuiеs – 48,6%, а также Cladosporium. Образцы семян из Северо-Казахстанской области были инфицированы альтернариозной инфекцией до 74%, гельминтоспориозной – от 7 до 32%. Пораженное альтернариозом зерно – крупное, прорастает нормально, заболевание не передается семенами и отсутствует связь его с корневой гнилью. При анализе технологических свойств зерна, пораженного альтернариозом, установлено, что оно по хлебопекарным качествам не отличается от контрольного (Городилова, 1972; Коршунова, 1972).
Видовой состав возбудителей «черного зародыша» зависит от почвенно-климатических условий. Из пораженных семян яровой пшеницы из горно-степной и лугово-степной зон Восточно-Казахстанской области больше выделялся A. tenuies, степной – H. sativum. Образцы её семян, полученные из Костанайской, Павлодарской, Семипалатинской, Акмолинской областей инфицированы альтернариозной инфекцией до 50-70%, гельминтоспориозной – от 7 до 32% (Орынбаев, Федосимова, 1968).
В Западной Сибири на пшенице больше встречается гельминтоспориозный «черный зародыш», приводящий к щуплости и снижению всхожести семян. В то же время, при поражении их альтернариозом и кладоспориозом, всхожесть оставалась высокой. В связи с этим предлагалось вместо термина «черный зародыш» использовать «гельминтоспориоз» и «альтернариоз» зерновки (Гешеле, 1955). В Восточной Сибири гельминтоспориозный «черный зародыш» проявляется в годы с теплой погодой и выпадением обильных осадков в фазу налива зерна. При ГТК в июле от 0,7 до 1,2 гриб H. sativum развивается на междоузлиях стебля, вызывая корневую гниль, а при 1,3-1,6 происходит поражение зерна и корневой системы. При температуре 20-22°С в районах, где ГТК составляет 1,7-2,7 складываются благоприятные условия для поражения зерна гельминтоспориозным «черным зародышем» (Тупеневич,1970).
«Черный зародыш» зерна – широко распространенное заболевание пшеницы в Казахстане, особенно в северном и восточном регионах. В начале 60-х годов в зависимости от почвенно-климатических зон выращивания, в анализированных образцах пшеницы пораженных «черным зародышем» семян колебалась от 0,5-1 до 30,4%, заболевание больше было распространено в Восточно-Казахстанской и Кокшетауской областях (Орынбаев,1968).
Наши исследования в 1986-1988 гг. показали, что пораженность зерна пшеницы «черным зародышем» заметно колеблется в зависимости от сортовых особенностей пшеницы и погодных условий. В Южном Казахстане, где налив зерна озимой пшеницы происходит при высокой температуре и низкой относительной влажности воздуха, она не превышала 3,7-6,8%. В Костанайской, Северо-Казахстанской и Восточно-Казахстанской областях доля пораженных семян яровой пшеницы составляла от 15 до 23%, в Западно-Казахстанской – от 9 до 14,2%. Выявлена положительная связь (r= 0,40) между влажностью воздуха в период цветения и пораженностью зерна «черным зародышем», выражающаяся уравнением регрессии:
Y = 0,25X + 8,0 ± 2,8 ,
Она существенно не влияла на всхожесть семян, статистическая обработка данных выявила слабую коррелятивную связь между этими показателями (r=0,29). Семена озимой пшеницы, из Южного Казахстана, имели высокую всхожесть (97-99%), т.к. налив зерна и уборка проходят при низкой влажности воздуха (40-55%), выпадают не более 10-30 мм осадков. Семена яровой пшеницы, выращенные в северном и восточном регионах республики, имели всхожесть 90-95%, т.е. соответствовали требованиям 2 и 3 классов. Некоторое её снижение связано с более высокой инфицированностью их явной и скрытой инфекцией патогенных грибов, особенно B. sorokiniana. Корреляционно-регрессионным анализом выявлена определенная связь между пораженностью зерна «черным зародышем» и всходами корневой гнилью коэффициентом корреляции r= 0,46 и детерминации – 0,21 (Койшыбаев, Исмаилова, 1989). Однако, последняя, как правило, в 2-4 раза выше, что свидетельствует о скрытой зараженности семян гельминтоспориозной инфекцией [табл. 14].
Таким образом, вредоносным является гельминтоспориозный тип «черного зародыша». В связи с этим, важно уметь определить видовой состав возбудителей, что легко осуществляется в лабораторных условиях. При температуре 20-25°С инкубированные во влажной камере семена через 5-7 суток покрываются обильным темно-оливковым или сероватым налетом, состоящим из мицелия и спороношения гриба. По морфологии конидии легко можно их идентифицировать: у видов Alternaria они в длинных или коротких цепочках, яйцевидные, обратно–грушевидные, с поперечными и продольными перегородками, размером 20-63 × 9-18 мкм, короткой шейкой [рис. 13а]. У B. sorokiniana конидии одиночные, имеют только поперечные перегородки, прямые, обратно-яйцевидные, размером 14-34 × 20-130 мкм [рис. 13б].
Таблица 14. Влияние пораженности зерна «черным зародышем» на всхожесть семян пшеницы и пораженность всходов корневой гнилью
Фузариоз колоса является наиболее распространенной болезнью пшеницы в Западной Европе, Белоруссии, Европейской части Российской Федерации. Заболевание проявляется в период налива зерна, колосковые её пленки покрываются белым или розоватым налетом, состоящим из мицелий и спороношения грибов рода Fusarium. Возбудитель болезни представлен 19 видами, наиболее доминирующими являются F. sporotrichoides, F. poae, F. avenea. Высокопатогенные F. graminearum и F. culmorum, вызывающие щуплость и снижение всхожести, слабопатогенные F. poae F. equiseti, они локализуются на поверхности зерновки, не влияют на посевные качества семян, хотя выделяются часто. Первый вид распространен на Севером Кавказе, Дальнем Востоке, Северо-Западном регионе России (Гаккаева, Дмитриев, 2012; Левитин, 2012). В Белоруссии озимые зерновые культуры поражаются фузариозом до 60-70%, основными возбудителями являются F. oxysporum, F. culmorum и F. sporotrichiella Буга с соавт., 2006).
Рисунок 13. Конидии Alternaria tenyies (а) и Bipolaris sorokiniana (б)
Грибы рода Fusarium широко специализированы и вызывают корневую гниль однодольных и двудольных растений. Инфекция сохраняется на послеуборочных остатках растений, присутствует в почве, вызывая корневую гниль, передается семенами. При сильном поражении колоса урожай пшеницы снижается до 50%, ухудшаются посевные качества семян и технологические свойства зерна. Встречаются высокотоксичные виды рода Fusarium, при присутствии 5% пораженных ими зерен, продукция не пригодна для пищевых целей.
Некоторые сапрофитные организмы, развивающиеся на зерна при высокой влажности, могут выделять токсические вещества. Например, по данным ученых Германии, у афлотоксинов, продуцируемых плесневыми грибами, для крыс при введении орально ЛД50 составляет 7,2, а для фузарина, выделяемого возбудителем фузариоза зерна – 4,4 мг/кг (Шпаар,1994).
Энзимно-микозное истощение семян (ЭМИС)
Возбудители болезни – Cladosporium herваrum (Pers.) Lk, Alternaria alternata (Fr.) Keisl. Болезнь под названием «истекание», «черная плесень», «кладоспориоз» известна давно. В 1949 и 1950 гг. на Шортандинской опытной станции в начале восковой спелости зерна кладоспориозом поражалось от 43,4 до 62,3% колосьев пшеницы, в период уборки – до 90-100%, что было обусловлено высокой влажностью воздуха и частыми осадками (Джиембаев, Городилова, 1955).
М.С. Дунин и С.К. Темирбекова (1981) всесторонне анализировали этиологию энзимно-микозного истощения семян пшеницы. Установлено, что заболевание протекает в 3-х стадиях.
Первая стадия. при высокой влажности воздуха и выпадении обильных рос или дождя в фазу налива зерна резко возрастает активность гидролитических процессов, усиливается интенсивность дыхания, часть запасного крахмала и белка превращается в водорастворимые вещества. В клетках зерновок повышается гидростатическое давление, что приводит к микроскопическим разрывам оболочек. Через трещины вытекают из зерна водорастворимые вещества в виде «сладкой росы» или «медвяной росы». Эта стадия болезни может наступить в любой момент – с фазы молочной спелости до полного созревания зерна. С наступлением сухой погоды реактивация амилазы и протеазы прекращается, за счет фотосинтеза израсходованные на гидролитические процессы запасные вещества полностью или частично восстанавливаются.
Вторая стадия. Водорастворимые сахара и азотистые вещества, образующиеся при реактивации амилаз и других ферментов, являются хорошим субстратом для сапрофитных грибов и бактерий, развивающихся на поверхности колоса и зерна, которые в свою очередь выделяют ферменты, усиливающие распад запасных питательных веществ зерна, а также токсины, снижающие всхожести семян.
Третья стадия. При длительном увлажнении зерна и высокой температуре под влиянием гибереллина происходит синтез амилазы, которая индуцирует преждевременное прорастание его на корню в колосьях, а также под валками или во влажном ворохе.
ЭМИС имеет 2 формы: инфекционную и неинфекционную. При высокой влажности воздуха за счет увеличения гидростатического давления и активности ферментов происходят деформация и травмирование зерновки, это неинфекционное течении болезни. В инфекционной её стадии участвуют сапрофитные и паразитные грибы, в частности виды Cladosporium, Alternaria, Fusarium и Bipolaris sorokiniana.
Пшеница часто подвергается энзимно-микозному истощению в Центральной черноземной и нечерноземной зонах Российской Федерации, лесостепной зоне Западной Сибири, в отдельные влажные, в период молочно-восковой и восковой спелости, годы проявляется и в северном регионе Казахстана. В 1978-1985 гг. в Западной Сибири общий недобор её урожая от ЭМИС составлял 13-19%, с варьированием от 10 до 28% или от 2 до 9 ц/га. Кроме того, снижались технологические свойства зерна: масса зерна на 13-16,3%, натура – 56-86 г/л, содержание белка – 1,2-1,8% и качество клейковины, а также посевные качества семян: энергия прорастания – до 20%, лабораторная всхожесть – 10%, полевая – 25%, суммарная вредоносность болезни достигала 25-35% (Чулкина, 1984; Алимов, 1988).
В северном регионе республики заметное поражение колосьев пшеницы кладоспориозом происходило в наиболее увлажненные годы в период налива зерна, 2013-2016 гг. (Койшыбаев, 2016).
Спорынья
Возбудитель болезни – Claviceps purpurea Tul. из семейства Clavicipitiaceae. Грибы этого рода известны как продуценты эргоалколоидов, что связано с синтезом гистидина и триптофана (Гжехчек, 1976). Заболевание проявляется на колосьях в виде склероциев или рожков от фиолетового до черного цвета (длина 3-4 см), образующихся вместо зерна [рис. 14]. Они сохраняются на поверхности почвы или попадают в неё при посеве семян, весной прорастают, образуя красноватые стромы диаметром до 3-4 мм, в каждой из которых содержится 200-300 плодовых тел – перитеций с сумками и сумкоспорами. В период цветения зерновых культур последние выбрасываются из сумок и разносятся ветром. Попадая на колосья споры прорастают и через рыльце проникают в завязь цветка, уничтожая формирующееся зерно. В результате обильного конидиального спороношения гриб на завязи выделяет сладковатую жидкость или медвяную росу, которая привлекает насекомых. Таким путем заболевание распространяется очень быстро, мицелий гриба разрастается и превращает завязь в склероций.
Рисунок 14. Колосья озимой ржи, пораженные спорыньей
Многолетние наблюдения в юго-восточном, северном и восточном регионах показали, что в отдельные годы она проявляется на озимой ржи, ячмене, дикорастущих злаках, озимой и яровой пшенице встречается крайне редко. В Северном Казахстане пораженность ячменя спорыньей не превышала 0,5-0,8%, заболевание на яровой пшенице не обнаружено. В Западной Сибири поражаются ею озимая рожь и пшеница, особенно твердые сорта, из многолетних злаков – костер и пырей ползучий. Зерно с примесью спорыньи более 0,5% непригодно для размола на муку и кормления животных, содержит высокотоксичные алкалоиды. Для очистки семян от рожков спорыньи применяются подбор сит на специальном пневматическом сортировальном столе, а также метод погружение в раствор солей или селитры по удельному весу (Гешеле, 1956).
Бактериальные, вирусные и нематодные болезни
Пшеница, наряду с грибными поражается бактериальными и вирусными болезнями, возбудители которых широко специализированы, развиваются на многих дикорастущих злаках, что осложняет эффективную защиту посевов от патогенов.
Бактериальные
Возбудителями являются палочковидные бактерии, относящиеся к родам Pseudomonas, Xanthomonas и Bacillus. В Центральной черноземной зоне России на озимой пшенице встречаются 3 вида бактериальных болезней (бактериоза) – черный, базальный и бурый, которые различаются по симптомам проявления и видовому составу возбудителей. В Воронежской области распространение черного бактериоза колебалось от 7 до 51%, базального – с 21 до 75, бурого – с 13 до 52%. Зараженность семян пшеницы черным бактериозом достигала 20-30%, распространение болезни на её посевах до 42% (Шнейдер и Илюхина, 1975).
Черный или базальный бактериоз. Возбудитель болезни – Pseudomonas syringae pv. atrofaciens (синоним P. atrofaciens). Бактерии – подвижные палочки размером 0,5-0,8 × 1-2,5 мкм, с закругленными концами, одним полярным жгутиком. На картофельном агаре они образуют ярко-желтые слизистые колонии. Поражаются все надземные органы пшеницы: на листьях появляются темно-зеленые, просвечивающиеся водянистые пятна, которые позже становятся темно-коричневыми или черными, на стеблях – коричневые или черные продольные полосы. Признаки болезни на колосках проявляются у основания чешуи в виде полупрозрачных пятен. При сильном её развитии чернеет и деформируется весь колос, искривляется стебель, формируется щуплое зерно. Всходы от пораженных семян отстают в росте, часто погибают. Заболевание распространено на озимой и яровой пшенице в регионах с достаточно влажным климатом: на Украине, в Краснодарском крае, Центральной черноземной зоне России. Урожай у пораженных черным бактериозом растений может снижаться от 15 до 90%. Основной источник инфекции – зараженные семена и пожнивные остатки, где возбудитель сохраняется до следующего года. В период вегетации пшеницы инфекция распространяется каплями дождя, насекомыми с колюче-сосущим аппаратом (Илюхина, 1980; Королева, Чумаевская, 1983). В Акмолинской области на яровой пшенице обнаружена бактериальная пятнистость, вызываемая широкоспециализированной бактерией Pseudomonas syringae van Hall, которой поражаются также сорго, суданская трава, кукуруза и просо (Чумаевская, Городилова, 1974). Наши исследования показали, что она заметно проявляется на суданской траве и просо, при инокуляции пшеница поражается в слабой степени. При многократных анализах её семян, полученных из различных регионов республики, бактериальная инфекция не выявлена (Койшыбаев, Исмаилова,1989).
Бактериальная пятнистость. Возбудитель болезни – Xanthomonas campestris pv. translucens. Проявляется на листьях в виде водянистых пятен, которые позже становятся коричневыми. В 2002 г. впервые обнаружено заметное поражение яровой пшеницы бактериальной пятнистостью в Акмолинской области, которая проявлялась на листьях. Позже она обнаружена в ОПХ «Заречное» Костанайского НИИСХ на сорте Омская 24, и ячмене, который поражался болезнью в сильной степени. В 2005 г. бактериальная пятнистость была обнаружена в Тайыншинском и Аккайынском районах Северо-Казахстанской области на сортах пшеницы Омская 19, Астана, Астана 2 и Памяти Азиева. Заметное её развитие происходило в 2007-2008 и 2015 гг. на посевах опытной станции в период колошения пшеницы. Заболевание проявляется в период флаг-листа – колошение – цветение пшеницы в виде водянистых прозрачных полос и штрихов, расположенных вдоль главной жилки листьев. Позже они становятся коричневыми, на их поверхности образуется желтый экссудат бактерии, который при сухой погоде засыхает и крошится [рис. 15]. Вероятно, в распространении инфекции определенную роль играют насекомые, особенно сосущие вредители: злаковые тли, пшеничный трипс, цикады.
Рисунок 15. Листья пшеницы, пораженные полосчатым бактериозом
Слизистый или желтый бактериоз.
Возбудитель болезни – бактерия Rathayibacter tritici (Carls. et Vidav) Zgurskaia et all. (син.: Clavibaсter iranicus (Carls. et Vidav), Corynebacterium tritici Hutch.,Phytomonas tritici Elliott, Agrobacterium tritici Savul.)
Симптомы болезни, распространение, морфологические и биологические особенности возбудителя. Поражаются листья и их влагалище, где появляются продолговатые белые или желтые полосы, позже они скручиваются. У больных растений сильно деформируются колосья, часто они остаются в пазухе листьев, превращаясь в бесформенную слизистую массу. При влажной погоде на пораженных болезнью органах растений образуется желтоватый экссудат, который при сухой погоде высыхает, становится белым. Больные растения часто не выколашиваются и погибают. Возбудитель болезни – бактерии: подвижные палочки, с закругленными концами, одним полярным жгутиком, спор не образуют, размером 0,8-2,4 × 3,2 мкм. На мясо-пептоновом агаре образуют желтые, округлые, выпуклые колонии; на картофельном – бледно-желтые. Редуцируют глюкозу, фруктозу и глицерин, не усваивают манит и салицин; не гидролизуют желатин и крахмал, не образуют сероводорода, но выделяют аммиак. Одним из отличительных признаков бактерии от фитопатогенных видов является грамположительная реакция. Оптимальная температура для её роста находится в пределах 20-30°С, при 50°С теряет жизнеспособность (Израильский,1979).
Заболевание впервые обнаружено в 1917 г. в Индии, позже распространилось в Азиатский субконтинент, в частности Китай, Египет, а также в Северную Африку и Австралию. В странах СНГ отсутствует, является карантинным объектом. В 1999 г. обнаружено в Жамбылской области на сорте пшеницы, семена, которого были завезены из Египта. Для ликвидации очага карантинной болезни посевы были сожжены и участок перепахан, в дальнейшем она не выявлена.
Инфекция её передается семенами, распространяется нематодой Anguina tritici. Однако в Северной Америке, где распространена эта нематода, слизистый бактериоз на пшенице не обнаружен. Возможен занос инфекции воздушным потоком, а также насекомыми. При отсутствии растения-хозяина продолжительное время бактерия сохраняется на растительных остатках, переносится поливной водой на значительные расстояния.
В связи с вступлением Казахстана в ВТО и расширением торговли со странами Азии и Африки, вероятность проникновения патогена очень высокая. В связи с этим семена пшеницы, завозимые из стран, где распространен слизистый бактериоз, обязательно должны проходить фитоэкспертизу и высеваться для грунт-контроля в карантинном питомнике. Обеззараживание их от инфекции осуществляется термической обработкой при температуре 50-55°С или бактерицидным препаратом. При обнаружении очага болезни нужно сжигать посевы пшеницы или обработать их гербицидом сплошного действия, вспахать почву с оборотом пласта на глубину не менее 20-25 см.
Вирусные болезни
На пшенице встречаются русская мозаика озимой, полосатая мозаика яровой пшеницы и красная полосчатость листьев сорго. Возбудители их широко специализированы, наряду с основным хозяином поражают многие культурные и дикорастущие злаки. Некоторые вирусы передаются семенами, многие распространяются при контакте больных растений со здоровыми, а также орудиями труда, насекомыми-переносчиками. По способу передачи вирусы делятся на 3 группы: персистентные, полуперсистентные и неперсистентные, которые легко распространяются механическим путем. Переносчиками многих вирусных болезней являются тли при непродолжительном контакте (1-2 мин.) с больным растением. Персистентные вирусы переносятся цикадами, которые инфицируются при продолжительном (до нескольких часов) питании на больном растении и переносят инфекцию после определенного инкубационного периода. Полуперсистентные вирусы занимают промежуточное положение. Установлено, что возбудителями некоторых болезней типа желтухи являются не вирусы, а микоплазменные тела, которые в отличие от вирусов, размножаются на искусственных питательных средах сложного состава, по форме они эллипсоидальные или округлые, размером 200-300 нμ (Власов, Ларина, 1982).
Мозаика (русская) озимой пшеницы. Возбудитель болезни – Triticum virus 8, вирионы – бацилловидной формы длиной 240-2 880, шириной 55-65 нμ. Наиболее характерный признак болезни – мозаичность в виде узких светло-зеленых и желтых или лимонно-желтых полос и штрихов, располагающихся вдоль жилок листьев. Отличительным признаком вируса является образование игловидных кристаллов при мацерации кусочка больных листьев в капле раствора 0,1 N HCl, однако, он не является стабильным. Вирус поражает яровую пшеницу, просо, ячмень и озимую рожь, из дикорастущих злаков – щетинник (Setaria glauca Beauv., S. viridis Beauv.), а также вейник наземный (Calamagrostis epigeios). Озимая пшеница и рожь инфицируются с осени; переносчики болезни – полосатая и темная цикадки (Psammotettix striatus L. и Macrosteles laevis).
Полосатая мозаика пшеницы. Возбудитель болезни – Triticum virus. Характерный признак болезни – слабые хлоротичные полосы и штрихи вдоль жилок листьев, часто расширяющиеся и сливающиеся [рис. 16].
При сильном поражении растений зерно не формируется. Переносчики болезни – клещи Aceria tulipae Keif. и A. tritici Schev., инфекция легко передается при контакте здоровых растений с больными. Вирус сохраняется на озимой пшенице, весной векторы переносят его на яровые, поражаются просо, озимая рожь, овёс, виды щетинников и костра. Заболевание широко распространено в республиках Центральной Азии, в частности в Узбекистане (Горбунова, 1966). В Казахстане встречается в южном и юго-восточном регионах. В Костанайской области наблюдали очень сильное поражение этой болезнью озимой пшеницы и костра.
Рисунок 16. Листья пшеницы, пораженные мозаикой
Закукливание злаков. Характерный признак болезни – усиленное кущение больных растений, сильное отставание в росте, карликовость. Переносчиком болезни является цикада – Laodelphax striatellus Fall., зимующая на стерне диких злаков, весной заражающая яровые зерновые культуры, а также виды мышея и других злаковых трав. Закукливание широко распространено в Сибири и на Дальнем Востоке. В начале 60-х годов прошлого столетия в Северо-Казахстанской области распространение болезни на яровой пшенице варьировало от 1-3 до 10-25% в зависимости от сроков посева и сорта (Джиембаев, 1974).
В последние десятилетия в Поволжье и других регионах России большее распространение приобретают на пшенице вирусные болезни, в частности, русская мозаика озимой пшеницы, мозаика костра безостого; микоплазменные – желтая карликовость ячменя, бледно-зеленая карликовость пшеницы. На яровой пшенице степень их распространения составляла 10-15%, на озимой – 25-30%. Вредоносность вирусных и микоплазменных болезней зависит от ряда факторов, одним из основных является время заражения растений. При проявлении их в фазе 2-3 листьев происходит значительный недобор урожая, иногда полная гибель растений. Заражение озимых зерновых проявляется в весенний период, как правило, в виде мозаичности листьев, из-за щуплости зерна и частичной стерильности цветков колоса продуктивность больных растений снижается заметно. Переносчиками вирусных болезней в основном являются разные виды тлей, микоплазменных – цикады, одной из главных причин вспышки указанных болезней являются высокая их численность. Поэтому главное значение имеет химическая защита посевов пшеницы от насекомых, пространственная изоляция яровой пшеницы от озимых зерновых, оптимальные сроки и нормы посева (Маркелова с соавт., 2012).
Нематодные болезни
Нематоды или круглые черви, в основном обитают в почве, некоторые виды паразитируют на растениях, образуя галлы или цисты, различные наросты. Они развиваются из яиц, размножаются половым или партеногенетическим путем, проходят четыре стадии.
Галловая или пшеничная нематода зерна. Возбудитель болезни – Anguina tritici (Stein.) Chitwood – переносчик слизистого бактериоза пшеницы.
В период её вегетации проявляется в виде искривления стеблей и деформации листьев. Заражение зерна происходит в период формирования, внутри колоска образуются темно-коричневые галлы, не отличающиеся по форме от семян пшеницы. Внутри них находятся личинки нематод, которые попадают в почву при уборке и сохраняются в виде примесей к семенам. Осенью или весной при посеве семян из галлов выходят тысячи личинок нематод и заселяют розетки листьев и нижнюю часть стебля. Далее они проникают в завязь пшеницы, где откладывают яйца, превращая зерновку в галлы. Паразитирует на пшенице, озимой ржи, тритикале и некоторых дикорастущих злаках. Распространена в странах с влажным климатом: субконтиненте Индия, Восточной Америке, Западной Европе, Восточной и Южной Азии (Дувейллер, Сингх, с соавт., 2014). В Казахстане не выявлена.
Нематоды, поражающие корневую систему – Heterodera avenea, Meloidogyne spp., Pratylenchus spp. Цистообразующие нематоды развиваются чаще на корневой системе всходов, которая утолщается и разветвляется, появляются наросты и цисты, вначале белые, по мере старения становятся темно-коричневыми. В каждом галле содержится несколько самок, которые откладывают большое количество яиц, из них в середине лета отрождаются личинки, которые сохраняются в почве в зрелых цистах, выходят из них и заражают проростки весной при высокой влажности почвы (Дувейллер, Сингх, с соавт., 2014).
При мелоидогенезе признаки болезни проявляются на верхней части корневой системы в виде мелких узлов и галлов. Пораженные растения отстают в росте, листья становятся хлоротичными, при высокой температуре происходит их увядание. Цистообразующие нематоды специализированы на злаковые растения, не поражают двудольные культуры, сохраняются в почве. Путем чередования культур в севооборотах можно ограничить их численность и развитие болезней.
Признаки поражения пшеницы видами Pratylenchus проявляются на корневой системе в виде небольших коричневых пятен, которые сливаются между собой, превращаются в некротизированные участки. Боковые корни разветвляются слабо, становятся тонкими, снижаются их количество и длина. Нематоды являются мигрирующими эндопаразитами, в период вегетации могут поражать корневую систему растений, свободно передвигаются по ней и в почве. Личинки проникают в цитоплазму растений, питаются их содержимым. Они широко специализированы и поражают и двудольные, в том числе ягодные и садовые культуры. Вид Pratylenchus thornei специализирован на пшеницу, хорошо развивается на легких почвах при засушливых условиях погоды, вызывая потери урожая до 85% (Дувейллер, Сингх и др., 2014). Поэтому этот вид представляет серьезную опасность для пшеницы в Центральной Азии. При многолетних исследованиях корневых гнилей пшеницы в разных почвенно-климатических зонах Казахстана, нематодные болезни не обнаружены.
Грибы
Грибы — царство эукариотических одноклеточных и многоклеточных гетеротрофных организмов, имеющих ряд общих черт с растениями и животными, но и ряд особенностей, которые отличают их от упомянутых царств. По способу питания грибы могут быть сапротрофами и паразитами.
Строение грибов
Ключевыми особенностями клетки гриба является наличие клеточной стенки из хитина. Запасным питательным веществом, как и у животных, служит гликоген. В пищевых цепях грибы занимают позицию редуцентов, разрушая органические вещества мертвых животных и растений. К фотосинтезу грибы не способны (у них отсутствуют пластиды — хлоропласты), неподвижны, дышат кислородом.
Некоторые грибы образуют плодовые тела, в обиходе называемые — грибы. Плодовое тело служит для образования спор в ходе полового процесса.
Тело гриба состоит из нитей — гифов, которые многократно переплетаются друг с другом, в результате чего образуется мицелий (греч. mykes — гриб), или грибница. Гифы гриба разрастаются в питательной среде, на субстрате, и представляют собой вегетативные органы гриба.
Рост гриба ни чем не ограничен, только размером самого субстрата. Таким образом, если мы представим себе буханку хлеба размером с земной шар и благоприятными условиями, то плесневый гриб, мукор, занял бы все это пространство, пока субстрат не закончился.
Гифы грибов, сплетаясь с корнями растений образуют микоризу (греч. mykes — гриб + rhiza — корень), или грибокорень. Это особая форма взаимоотношений между видами — симбиоз (точнее — мутуализм), при котором оба организма извлекают взаимную выгоду из отношений.
Гифы гриба увеличивают площадь всасывания воды из почвы для растения: гриб делится водой с зеленым другом)) А растение в процессе фотосинтеза создает органическое вещество, которым делится с грибом, что оказывается весьма полезно для него.
Сходство грибов и животных
Сходство между грибами и животными заключается в следующем:
И для животных, и для грибов характерен гетеротрофный тип питания — поглощение готовых органических веществ.
Как и у животных, конечным продуктом обмена веществ у грибов является мочевина.
В состав клеточной стенки грибов входит тот же биополимер (полисахарид) — хитин, который образует наружный скелет членистоногих.
Запасным питательным веществом грибов и животных является гликоген.
В клетках грибов, как и животных, отсутствуют пластиды: хлоропласты, лейкопласты, хромопласты — они встречаются только в клетках растений.
Высшие и низшие грибы
Все грибы подразделяются на высшие и низшие. Это разделение основано на строении мицелия: у низших грибов мицелий не имеет перегородок (неклеточный), гифы могут отсутствовать. К ним относятся мукор, фитофтора, стригущий лишай.
Высшие грибы имеют мицелий, разделенный перегородками (септами), могут образовывать плодовые тела. К высшим грибам относятся пеницилл, дрожжи, спорынья, шляпочные грибы.
Размножение грибов
Возможно вегетативное, бесполое и половое размножение. Вегетативное осуществляется с помощью деления мицелия на отдельные части: из каждой части в дальнейшем разрастается гриб.
Бесполое размножение происходит благодаря спорообразованию. На концах гиф или в спорангиях (на конидиеносцах) образуются споры. Конидиеносцы представляют собой разветвленные концевые участки гиф. Спора, попав в благоприятную среду, прирастает и дает начало новому мицелию гриба.
Половое размножение заключается в образовании сперматозоидов в антеридиях и яйцеклеток в оогониях. После образования зиготы (2n) у многих грибов сразу же происходит зиготическая редукция — зигота делится мейозом, образовавшиеся клетки имеют гаплоидный (n) набор хромосом.
У сумчатых грибов в плодовых тела развиваются специальные сумки (аски), в которых образуются гаплоидные споры. Они прорастают в мицелий, на котором из антеридиев образуются сперматозоиды (n), а из овогний — яйцеклетки (n). При их слиянии образуется зигота (2n), которая три раза делится мейозом на 8 аскоспор (n).
У базидиомицет (мухомор, сыроежка, подосиновик красный, подберёзовик, шампиньон, опенок, рыжик, лисичка) сумки отсутствуют. Размножение происходит с помощью базидиоспор, которые развиваются на базидиях открыто. У них происходит соматогамия — слияния 2 клеток вегетативного мицелия.
Особо отметим дрожжи, которые способны к почкованию. При почковании на клетке появляется утолщение, которое постепенно растет и превращается в полноценную дочернюю особь.
Грибы паразиты и возбудители болезней
Около 30-40% грибов являются паразитами и возбудителями болезней растений и животных. Заболевания, которые вызывают грибы, носят название — микозы.
Паразитирует на злаковых растениях. При поражении растения на месте плодов (зерновок) вырастают черные образования — склероции, по своему строению являющиеся переплетениями гифов гриба. Спорынья может заразить новые растения, если ее споры достигнут завязи пестика.
Склероции содержат токсичные вещества, которые, если попадут в муку, могут привести к серьезному отравлению человека вплоть до летального исхода.
Эти грибы способны вызывать заболевания пшеницы, кукурузы, ржи. Внешне заболевание проявляется черными, кажущимися обугленными колосками, которые в действительности наполнены спорами гриба черного цвета.
В цикле развития этого паразита присутствуют два хозяина: «весенний» — барбарис, «летний» — пшеница и другие злаки. Споры характерного красно-ржавого цвета в количестве нескольких поколений образуются за одно лето.
Эти споры покрывают листья и стебли, их внешний вид напоминает ржавчину. К зиме споры темнеют и становятся черными, после перезимовки цикл повторяется заново.
Гриб проникает в клетки растений и питается их содержимым, приводя к гибели растения. Внешне проявляется как белый пушок на листьях, клубнях (у картофеля). Со временем темнеет из-за разрушения клеток растения.
Мучнистая роса значительно снижает урожаи картофеля, томатов и других культурных растений.
Фитофтора относится к низшим грибам. Гриб проникает в клетки подземных и надземных органов растений, питается их содержимым, приводя к увяданию, усыханию и гибели растения. Внешне проявляется как пятнышки буро-серозного цвета, окруженные кольцом белого цвета.
Фитофтора снижает урожаи картофеля, баклажанов, томатов, перца, клубники и других культурных растений.
Шляпочные грибы
Шляпочные грибы особенны тем, что помимо грибницы способны образовывать плодовые тела, которые состоят из шляпки и ножки. Нижняя сторона шляпки может напоминать отверстия тонких трубочек или пластинок.
Из-за такой разницы во внешнем виде все грибы делятся на трубчатые и пластинчатые. К трубчатым грибам относятся: подберезовик, масленка, белый гриб. К пластинчатым: опенок, сыроежка, рыжики, шампиньоны, волнушки.
На пластинках и трубочках образуются споры, которые падают на землю и, попав в благоприятные условия, прорастают в мицелий. Из мицелия вновь вырастает плодовое тело.
Разветвленные гифы гриба всасывают из почвенного раствора необходимые воду и минеральные вещества. Часто грибы могут расти только образовав микоризу с корнями деревьев, для них такой симбиоз — единственный источник органических веществ.
В то же время другим грибам, например шампиньонам, образование микоризы совершенно необязательно. Эта особенность физиологии делает шампиньоны отличным вариантом для искусственного разведения.
Среди шляпочных грибов выделяют съедобные грибы (волнушка, сыроежка, лисичка, масленок) и ядовитые. Наиболее ядовиты следующие грибы: бледная поганка, мухоморы, ложные лисички, ложные опята.
Антибиотики
Открытие пенициллина — первого антибиотика, вырабатываемого грибом пенициллом — чистая случайность, спасшая десятки миллионов жизней! Эта «революция» случилась 28 сентября 1928 года, в лаборатории блестящего исследователя (и к счастью — чрезвычайного растяпы!) Александра Флеминга.
В августе 1928 он отправился в отпуск с семьей, и неопрятно положил в углу своего стола лабораторную посуду с колониями стафилококка. Вернувшись из отпуска 3 сентября 1928 года, он обнаружил, что на одной пластине со стафилококками появились плесневые грибы.
Удивительно, но стафилококки погибали и не могли расти и размножаться вокруг плесени. Неизвестное химическое вещество (позднее названное пенициллином) останавливало размножение бактерий. Это было открытие первого антибиотика, который показал потрясающий результат: стало возможным лечение многих инфекционных болезней, больные обретали вторую жизнь с помощью гениального изобретения природы — антибиотиков.
Лишайники
-
Накипные (корковые) — практически неотделимы от субстрата, срастаются с ним
Представители накипных лишайников: лицедея, леканора.
Представители листоватых лишайников: пармелия, ксантория.
Представители кустистых лишайников: ягель (олений мох), кладония, цетрария (исландский мох).
Хочется предупредить частую ошибку. В тундре произрастает олений мох — на самом деле никакой он не мох! Это лишайник, по-другому олений мох называется ягель. Этот кустистый лишайник служит основным источником корма для северных оленей.
Лишайники являются маркером: они растут преимущественно в экологически чистых местах, в городских условиях встречаются редко.
© Беллевич Юрий Сергеевич 2018-2021
Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение (в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования, обратитесь, пожалуйста, к Беллевичу Юрию.
Грибная лилипутия — от паразитов до хищников
Грибы — одни из самых удивительных и загадочных живых существ — недаром выделены в отдельное царство наравне с растениями и животными. Систематически все грибы относятся к микроорганизмам, и огромное большинство из них действительно можно увидеть невооруженным глазом только тогда, когда они разрастаются на подходящем субстрате, образуя колонии (плесени).
Микроскопические грибы (микромицеты) практически вездесущи — их можно встретить везде: в атмосферном воздухе, почве, на стенах домов, даже на музейных экспонатах… Многие из этих малозаметных созданий представляют потенциальную опасность для здоровья людей и животных, являясь причиной возникновения микозов и аллергий.
Однако человек давно научился использовать их в своих целях, например, в виноделии и хлебопечении. Сегодня микроскопические грибы являются также продуцентами важнейших лекарств (антибиотиков) и биологически активных веществ. А такие удивительные создания, как хищные грибы, используются для разработки биологических средств защиты растений от вредителей. Задача ученых — продолжать поиск новых эффективных «биотехнологических» штаммов среди огромного разнообразия представителей третьего царства
Собирая в осеннем лесу крепенькие боровики, мы не задумываемся, что имеем дело не с самими грибами, а лишь с их плодовыми телами, пусть и крупными. Систематически все грибы относятся к микроорганизмам, и огромное большинство из них действительно можно увидеть невооруженным глазом лишь когда они образуют колонии, разрастаясь на подходящем субстрате. Этот огромный, невидимый микрокосм окружает нас. Вы найдете грибы везде: в воздухе и почве, в домах и на музейных экспонатах, и даже – в обычном утреннем бутерброде.
Среди высших организмов грибы составляют отдельное обширное царство*. Систематики выделяют в нем два отдела: слизевые грибы – Myxomycota, и собственно грибы (истинные грибы) – Eumycota, которые, в свою очередь, подразделяются на шесть классов. Неспециалисту разобраться во всех классификационных тонкостях грибного разнообразия невозможно, да и не нужно. К тому же и сами микологи для удобства делят все грибы, независимо от их систематической принадлежности, на две группы, согласно размерам – микро- и макромицеты.
Микромицеты (от греч. mikros – маленький и mykes – гриб) оправдывают свое название: большинство из них можно увидеть лишь с помощью микроскопа. Однако, разрастаясь на подходящем субстрате, микромицеты могут становиться видимыми невооруженным глазом, образуя всем известные «плесени». При этом они никогда не образуют крупных плодовых тел, как, например, шляпочные грибы, широко используемые в кулинарии и медицине.
Однако человек давно научился использовать в своих целях и эти малозаметные и не всегда презентабельные создания. Виноделие, хлебопечение – примеры первых биотехнологий, где нашли применение дрожжи, одноклеточные представители обширного класса сумчатых грибов (к этому же классу относятся сморчки и знаменитые трюфели). В историю сыроварения яркую страницу вписали грибы р. Penicillium, представители которого придают острый вкус и голубой мраморный окрас знаменитому рокфору. Этот же род открыл новую эру в лечении тяжелых бактериальных инфекций, дав миру антибиотики.
Сначала человек использовал дикие штаммы, но затем с помощью селекции, а потом и достижений генетики удалось получить высокоэффективные штаммы микромицетов, которые сегодня широко используются не только для получения вин, сыра и антибиотиков, но также органических кислот, ферментов, витаминов, кормовых добавок и т. п. Микроскопические грибы стояли и у истоков разработки биологических средств защиты растений от насекомых-вредителей, болезней и сорняков.
Но у каждой медали есть две стороны. Так, среди микромицетов есть много видов, способных вызывать различные заболевания у растений, животных и человека. Фактором риска для здоровья человека считается присутствие в жилых помещениях спор грибов родов Aspergillus, Cladosporium и Penicillium, поскольку некоторые их представители могут вызывать серьезные заболевания (микозы) либо аллергии (Иванова и др., 2007; Кононенко и др., 2008). Патогенные и аллергенные виды микроскопичеких грибов выделяют даже из музейного воздуха и выставочных экспонатов (Богомолова и др., 2007).
Таким образом, и полезные, и вредные для человека микроскопические грибы находятся прямо рядом с нами: в почве, воздухе, на стенах домов и т. п. Эти микроорганизмы, как показывают исследования, являются неотъемлемыми структурными и функциональными компонентами любых наземных экосистем.
Прямо из воздуха
Чтобы убедиться в вездесущности микромицетов, достаточно посмотреть результаты биологического мониторинга атмосферного аэрозоля юга Западной Сибири, который был проведен сотрудниками нескольких научных подразделений ГНЦ ВБ «Вектора» (Сафатов, Теплякова и др., 2009).
Среди грибов, обнаруженных в рассевах проб атмосферного воздуха, были идентифицированы представители 18 родов, не считая неопознанных. Доминирующими являются грибы родов Aspergillus, Penicillium, Cladosporium и Alternaria – все эти потенциально опасные для здоровья человека виды грибов характерны и для других регионов СНГ, от Аджарии до Санкт-Петербурга (Иванова и др., 2007; Верулидзе и др., 2008). Представители еще пяти родов являются фитопатогенными, т. е. вызывают заболевания у растений.
Однако в рассевах проб атмосферного воздуха обнаружились и колонии грибов, являющиеся потенциальными продуцентами различных биологически активных веществ. Например, темноокрашенные грибы, содержащие меланин, споры которых, как оказалось, присутствовали во всех пробах атмосферного воздуха.
Как известно, меланин (от греч. mеlanos – черный) – широко распространенный в природе темный пигмент, содержащийся в эпидермисе, волосах, сетчатке глаза и т. д.; именно этот пигмент в большом количестве образуется в нашей коже под действием ультрафиолетовых лучей. Но одним загаром его функции не ограничиваются: меланин не только является регулятором процессов клеточного метаболизма, но и играет роль универсального протектора при действии на клетку физико-химических факторов мутагенной и канцерогенной природы (Борщевская и др., 1999).
В настоящее время в Беларуси уже производятся мази от кожных заболеваний, в которых используется меланин, полученный из грибов (Литвинов и др., 2008). Занимаются грибными меланинами и иркутские исследователи (Огарков и др., 2008).
Среди грибов, часто встречающихся в рассевах и представляющих интерес для медицинской биотехнологии, хочется выделить р. Aureobasidium. На основе одного из видов этого рода в той же Беларуси уже начато промышленное производство нового плазмозаменяющего вещества (Литвинов и др., 2008).
За чужой счет
Колонии грибов, выросшие из рассевов атмосферного воздуха, часто представляли собой смесь из колоний двух и более видов, которые различались по форме и цвету. Внимательное исследование под микроскопом показало, что часто имело место паразитирование одного вида гриба на другом.
Термин «микофильность» обозначает способность организма развиваться в природе за счет грибов. Микофильными бывают вирусы, бактерии, актиномицеты… Но все эти организмы превосходят по числу видов и паразитической активности сами грибы, которые так и называются – микофилы. Численность этой группы, куда входят представители почти всех классов грибов, достигает 2 тыс. видов (Рудаков, 1981).
Микофильные грибы широко распространены в разных климатических зонах и во всех местообитаниях: в воде, почве, на плодовых телах и в мицелии макроскопических грибов, на поверхности и внутри мицелия различных микромицетов и т. д. Эти грибы играют в природных экосистемах важную роль: они способствуют разложению и минерализации грибных остатков и ограничивают численность популяций других грибов.
Микофилы являются естественными врагами фитопатогенных грибов, поэтому их используют в практике биологической защиты растений. Например, продуцентами биопрепаратов являются грибы р. Trichoderma, Ampelomyces и др. С другой стороны, микофилы представляют серьезную угрозу для культивируемых съедобных грибов – достаточно упомянуть белую гниль шампиньона, вызываемую грибом Mycogone pernicosa. Урожайность грибной культуры при таком заражении снижается вдвое и более.
Паразитические грибы могут играть отрицательную роль и в ряде других случаев, связанных с культивированием грибов: при поддержании коллекций грибных штаммов, когда колонии пересеваются на новые питательные среды; при производстве коммерческого мицелия. Стоит добавить, что развитие в России промышленного грибоводства привело к появлению большого числа лабораторий по производству посевного мицелия. И не секрет, что в таких лабораториях зачастую нет даже микроскопа, и вся оценка роста и качества мицелия проводится визуально, по цвету колоний и скорости зарастания среды.
Грибы-микофилы представляют особую опасность при выделении тканевых и споровых культур из природных или культивируемых грибов. Например, практически все штаммы съедобных грибов-базидиомицетов, отобранные в 1950—1970-е гг. для промышленного культивирования в целях получения грибной биомассы, оказались микофильными гифомицетами.
В результате культивирование таких штаммов породило ошибочные представления, что в глубинной культуре базидиомицетов образуются мутанты с несвойственным высшим грибам типом спороношения. Поскольку грибная биомасса, полученная в результате такого культивирования, не имела ожидаемого вкуса и аромата, это отрицательно сказалось на развитии исследований в области глубинного культивирования съедобных грибов (Бухало, 1998).
В результате исследований удалось установить, что микофильные грибы могут присутствовать в культурах многих съедобных и лекарственных грибов длительное время в форме мицелия (т. е. гифа паразита сохраняется в гифе базидиомицета) (Теплякова, 1999). Причем их присутствие в пересеваемых колониях долгое время может не проявляться – обнаружить его можно только при исследовании образцов под микроскопом.
Однако иногда гриб-паразит может получить преимущественное развитие. И специалист-миколог, не знакомый с особенностями жизнедеятельности микофильных грибов, не всегда может разобраться с причиной массового размножения другого гриба, а не культивируемого. Чаще всего это явление объясняется недостаточной стерильностью среды, однако причина лежит гораздо глубже.
В конечном счете культура базидиомицета может быть потеряна. Например, в Новосибирск из Казахстана был привезен запатентованный штамм шампиньона, продуцента биологически активного вещества. Автор штамма, опытный технолог, проводила контроль культуры гриба после его выделения из природы преимущественно визуально. В результате оказалось, что вместо шампиньона в качества продуцента БАВ давно используется микофильный гриб р. Verticillium.
Охотники за нематодами
Среди микромицетов хочется особо выделить одну экологическую группу грибов, эволюционно связанную с обычными обитателями почвы нематодами (круглыми червями). Эти удивительные грибы, которых формально можно отнести к паразитам, по повадкам – настоящие хищники.
Естественные враги нематод названы хищными грибами за их способность формировать на гифах мицелия различного вида приспособления для улавливания своих жертв. Поскольку хищные грибы обнаружены практически во всех частях мира, это свидетельствует, что в природе они играют важную экологическую роль, утилизируя огромную массу нематод, многие из которых являются возбудителями опасных гельминтозов растений и животных.
Вообще роль хищных грибов в природе еще в полной мере не изучена, хотя в последние годы была проделана большая работа по отбору из природы эффективных штаммов нематофаговых грибов, изучению их особенностей, а также разработке технологии получения биопрепаратов против разных видов фитопаразитических нематод и испытанию их в природе (Теплякова, Ананько, 2009а, б).
Однако и на этих маленьких хищников нашлась управа – все те же микофильные грибы. С этим явлением исследователи из «Вектора» столкнулись при выделении гифомицетов из почвы в культуру: детальное микроскопическое исследование показало, что гифы и конидии хищного гриба вследствие паразитирования в них микофила иногда практически лишаются своего «живого» содержимого. Хотя внешне разрастание паразита в колонии хищника могло проходить незаметно, часто оно приводило к вытеснению хозяина. В результате качество биопрепарата против нематод падало, и ожидаемого эффекта при внесении его в почву не наступало.
Но есть и обратные примеры. Так, в лаборатории антибиотиков МГУ изучался сибирский штамм хищного гриба Arthrobotrys longa как потенциальный продуцент фибринолитических ферментов. Однако тщательное всесторонее исследование штамма показало, что продуцентом этих ферментов был вовсе не хищный гриб, а сопутствующий ему микофил р. Cephalosporium.
Дальнейшая оценка трех изолятов микофильных грибов, выделенных из хищных грибов, подтвердили предположение, что истинными продуцентами фибринолитических ферментов являются такие грибы-паразиты (Теплякова, 1999). Возможно, что дальнейший поиск штаммов грибов с фибринолитической активностью следует целенаправленно вести именно среди группы микофильных грибов.
Среди высших организмов грибы являются рекордсменами по способностям адаптироваться к самым разным условиям окружающей среды. Развитая поверхность нитей-гифов, составляющих грибной мицелий, обеспечивает большую площадь поглощения питательных веществ путем абсорбции. Имея мощный ферментативный аппарат, грибы могут разрушать многие материалы, созданные человеком – деревянные конструкции, строительные материалы и даже авиационное топливо.
Учитывая опасность биоповреждений, в строительные нормативы с 1997 г. введен термин «биологически активные среды», а для проведения регламентных технических осмотров самолетов ученые предлагают нормативно ввести обязательные контрольные анализы топлива и топливных систем с использованием стандартных микологических и микробиологических методов.
Но. как уже неоднократно упоминалось выше, наши давние враги могут стать и нашими союзниками, в том числе и в борьбе с человеческими недугами. Конечно, пока грибы, в том числе микроскопические, не часто используют для фармакологических целей, поэтому задача ученых – продолжать поиск эффективных продуцентов биологически активных веществ среди огромного природного разнообразия.
Борщевская М. И, Васильева С. М. Развитие представлений о биохимии и фармакологии меланиновых пигментов // Вопросы медицинской химии. 1999. Т. 45, вып. 1. С. 13—23.
Огарков Б. Н., Огаркова Г. Р., Самусенок Л. В. Грибы – защитники, целители и разрушители. Иркутск: ГУ НЦ РВХ ВСНЦ СО РАМН, 2008. 248 с.
Рудаков О. Л. Микофильные грибы, их биология и практическое значение . М.: Наука ,1981. 160 с.
Сафатов А. С., Теплякова Т. В., Белан Б. Д. и др. Концентрация и изменчивость состава микромицетов в атмосферном аэрозоле юга Западной Сибири // Оптика атмосферы и океана. 2009. Т. 22, № 9. С. 901—907.
Теплякова Т. В. Биоэкологические аспекты изучения и использования хищных грибов-гифомицетов. Новосибирск. 1999. 252 с.
Патент № 2366178, РФ. Способ получения препарата на основе хламидоспор микроскопического гриба для борьбы с паразитическими нематодами растений и животных / Теплякова Т. В., Ананько Г. Г. // Бюл. № 25. 2009.
Теплякова Т. В., Ананько Г. Г. Хищные грибы-гифомицеты против паразитических нематод // Защита и карантин растений. 2009. № 6. С. 22—25.
В публикации использованы фото автора
*См. «НАУКА из первых рук». 2010. № 33 (3). С. 104—113
: 29 Сен 2010 , Чарлз Дарвин — великий популяризатор эволюционной идеи , том 34, №4